题目内容
15.盐酸、醋酸、碳酸钠和碳酸氢钠是生活中常见的物质,下列表述正确的是( )| A. | NaHCO3溶液中存在:c(OH-)═c (H+)+c (H2CO3) | |
| B. | 25℃时,将pH=2的盐酸与pH=12的氨水混合后,溶液呈中性,则消耗溶液的体积:V(盐酸)<V(氨水) | |
| C. | pH相等的盐酸和CH3COOH溶液稀释到相同的pH,盐酸稀释的倍数大 | |
| D. | 将0.2mol/L的NaHCO3溶液和0.1mol/L的醋酸钠溶液等体积混合,溶液中存在:c(Na+)═c(CH3COOH)+c(CH3COO-)+c(CO32-)+c(HCO3-)+c(H2CO3) |
分析 A.根据碳酸氢钠溶液中的电荷守恒、物料守恒分析;
B.氨水为弱碱,氨水的浓度大于盐酸,若溶液为中性,则需要的盐酸体积较大;
C.醋酸中稀释过程中电离程度增大,若稀释后溶液pH相等,则醋酸溶液稀释的倍数较大;
D.反应后溶质为等浓度的碳酸氢钠和醋酸钠,根据物料守恒判断.
解答 解:A.碳酸氢钠溶液中根据物料守恒知:c(Na+)=c (H2CO3)+c(HCO3-)+c(CO32-),根据电荷守恒知:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2 c(CO32-),二者结合可得:c(H+)+c(H2CO3)=c(OH-)+c(CO32-),故A错误;
B.25℃时,将pH=2的盐酸与pH=12的氨水混合后,由于氨水为弱碱,则氨水浓度较大,若溶液呈中性,则消耗溶液的体积:V(盐酸)>V(氨水),故B错误;
C.pH相等的盐酸和CH3COOH溶液稀释到相同的pH,由于在稀释过程中电离程度增大,若稀释相同倍数时,醋酸的pH减小,所以若稀释后溶液pH相等,醋酸稀释的倍数大,故C错误;
D.将0.2mol/L的NaHCO3溶液和0.1mol/L的醋酸钠溶液等体积混合,反应后溶质为等浓度的碳酸氢钠和醋酸钠,根据物料守恒可得:c(Na+)═c(CH3COOH)+c(CH3COO-)+c(CO32-)+c(HCO3-)+c(H2CO3),故D正确;
故选D.
点评 本题考查了离子浓度大小的比较,为高考常见题型,题目难度中等,试题侧重于学生的分析能力的考查,能运用物料守恒和电荷守恒是解本题的关键,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
14.下列有关化学用语正确的是( )
| A. | N2的电子式: | |
| B. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{78}$I | |
| C. | S2-的结构示意图: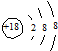 | |
| D. | 乙烯的结构简式:CH2═CH2 |
6.小明体检的血液化验单中,葡萄糖为5.9mmol/L.该体检指标的物理量是( )
| A. | 物质的量浓度 | B. | 溶解度 | C. | 质量分数 | D. | 摩尔质量 |
10.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 34g质量分数为4%的H2O2水溶液中含氧原子数目为0.08NA | |
| B. | 反应3H2(g)+N2(g)═2NH3(g)△H=-92kJ/mol,若放出热量4.6kJ,则转移电子数目为0.3NA | |
| C. | 常温常压下,28g乙烯与丙烯的混合气体中含有的碳原子数目无法计算 | |
| D. | 6.4gCu与40mL10mol•L-1浓硝酸作用能生成NO2的分子数为0.2NA |
20.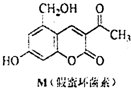 天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
 天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )| A. | M的分子式为C12H10O5 | |
| B. | M能发生取代反应、加成反应、氧化反应、还原反应 | |
| C. | M中碳原子之间全部以C-C键或C=C键相互结合 | |
| D. | M的同分异构体最多含有2个与乙酸相同的官能团 |
7.青蒿素在一定条件下可以合成双氢青蒿素,关于青蒿素和双氢青蒿素(结构如图)的下列说法中,错误的是( )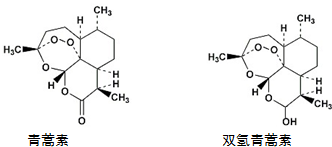

| A. | 青蒿素能发生还原反应 | |
| B. | 双氢青蒿素发生酯化反应和氧化反应 | |
| C. | 青蒿素分子中含有过氧链和酯基、醚键 | |
| D. | 双氢青蒿素分子中有2个六元环和2个七元环 |
4.下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
| A. | 0.1 mol/LNa2CO3溶液中:c(Na+)═(HCO3-)+c(H2CO3)+2c(CO32-) | |
| B. | pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 | |
| C. | 将0.2mol/LNaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)═c(A-)+c(Cl-) | |
| D. | 常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
5.A、B、C、D 均为气体,对于A+3B?2C+D 的反应来说,以下化学反应速率的表示中反应速率最快的是( )
| A. | v(A)=0.4 mol/(L•s) | B. | v(B)=0.8 mol/(L•s) | C. | v(C)=0.6 mol/(L•s) | D. | v(D)=0.1 mol/(L•s) |
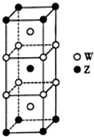 短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多.
短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多.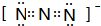 .
.