题目内容
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有白色沉淀生成,在所得的悬浊液中逐滴加入1mol?L-1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试回答:
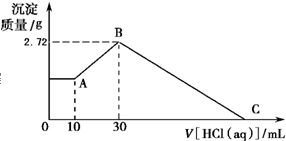
(1)从0开始到A点沉淀物的化学式为 ;B点沉淀物的化学式为 .
(2)原混合物中的MgCl2的物质的量为 ,AlCl3的物质的量为 ,NaOH的物质的量为 .
(3)HCl溶液在C点的体积数是 mL.

(1)从0开始到A点沉淀物的化学式为
(2)原混合物中的MgCl2的物质的量为
(3)HCl溶液在C点的体积数是
考点:有关混合物反应的计算
专题:计算题
分析:把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有白色沉淀生成,向所得的悬浊液中加入盐酸时,0-10mL时没有沉淀生成,说明溶液中NaOH过量,则铝离子完全转化为偏铝酸根离子,沉淀为Mg(OH)2.
则0-10mL发生反应:OH-+H+=H2O,A点时,溶液中溶质为NaCl、NaAlO2;
AB段发生反应:H2O+AlO2-+H+=Al(OH)3↓,B点溶液中存在的溶质是NaCl,沉淀为Mg(OH)2、Al(OH)3;
BC段发生反应:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O,C点时,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液.
(2)计算AB段生成氢氧化铝沉淀消耗HCl的物质的量,进而计算氢氧化铝的物质的量,根据沉淀质量计算氢氧化镁的质量,根据元素守恒计算氯化镁、氯化铝的物质的量;
B点溶液中存在的溶质是NaCl,根据钠离子、氯离子守恒可知,n(NaOH)=n(NaCl)=n(HCl)+2n(MgCl2)+3n(AlCl3);
(3)C点溶液为MgCl2、AlCl3和NaCl混合液,由氯离子守恒可知,氯化钠中氯离子源于加入盐酸,根据钠离子守恒可知m(NaOH)=n(NaCl),进而计算加入盐酸的体积.
则0-10mL发生反应:OH-+H+=H2O,A点时,溶液中溶质为NaCl、NaAlO2;
AB段发生反应:H2O+AlO2-+H+=Al(OH)3↓,B点溶液中存在的溶质是NaCl,沉淀为Mg(OH)2、Al(OH)3;
BC段发生反应:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O,C点时,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液.
(2)计算AB段生成氢氧化铝沉淀消耗HCl的物质的量,进而计算氢氧化铝的物质的量,根据沉淀质量计算氢氧化镁的质量,根据元素守恒计算氯化镁、氯化铝的物质的量;
B点溶液中存在的溶质是NaCl,根据钠离子、氯离子守恒可知,n(NaOH)=n(NaCl)=n(HCl)+2n(MgCl2)+3n(AlCl3);
(3)C点溶液为MgCl2、AlCl3和NaCl混合液,由氯离子守恒可知,氯化钠中氯离子源于加入盐酸,根据钠离子守恒可知m(NaOH)=n(NaCl),进而计算加入盐酸的体积.
解答:
解:把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有白色沉淀生成,向所得的悬浊液中加入盐酸时,0-10mL时没有沉淀生成,说明溶液中NaOH过量,则铝离子完全转化为偏铝酸根离子,沉淀为Mg(OH)2.
则0-10mL发生反应:OH-+H+=H2O,A点时,溶液中溶质为NaCl、NaAlO2;
AB段发生反应:H2O+AlO2-+H+=Al(OH)3↓,B点溶液中存在的溶质是NaCl,沉淀为Mg(OH)2、Al(OH)3;
BC段发生反应:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O,C点时,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液.
(1)由上述分析可知,从0开始到A点沉淀物的化学式为Mg(OH)2;B点沉淀物的化学式为Mg(OH)2、Al(OH)3,
故答案为:Mg(OH)2;Mg(OH)2、Al(OH)3;
(2)AB段生成氢氧化铝沉淀消耗HCl的物质的量为(0.03L-0.01L)×1mol/L=0.02mol,由H2O+AlO2-+H+=Al(OH)3↓,可知氢氧化铝的物质的量为0.02mol,则氢氧化镁的质量为2.72g-0.02mol×78g/mol=0.02mol,由元素守恒可知,n(MgCl2)=n[Mg(OH)2]=0.02mol,n(AlCl3)=n[Al(OH)3]=0.02mol;
B点溶液中存在的溶质是NaCl,根据钠离子、氯离子守恒可知,n(NaOH)=n(NaCl)=n(HCl)+2n(MgCl2)+3n(AlCl3)=0.03L×1mol/L+0.02mol×2+0.02mol×3=0.13mol,
故答案为:0.02mol;0.02mol;0.13mol;
(3)C点溶液为MgCl2、AlCl3和NaCl混合液,由氯离子守恒可知,氯化钠中氯离子源于加入盐酸,根据钠离子守恒可知m(NaOH)=n(NaCl)=0.13mol,C点加入盐酸的体积为
=0.13L=130mL,
故答案为:130.
则0-10mL发生反应:OH-+H+=H2O,A点时,溶液中溶质为NaCl、NaAlO2;
AB段发生反应:H2O+AlO2-+H+=Al(OH)3↓,B点溶液中存在的溶质是NaCl,沉淀为Mg(OH)2、Al(OH)3;
BC段发生反应:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O,C点时,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液.
(1)由上述分析可知,从0开始到A点沉淀物的化学式为Mg(OH)2;B点沉淀物的化学式为Mg(OH)2、Al(OH)3,
故答案为:Mg(OH)2;Mg(OH)2、Al(OH)3;
(2)AB段生成氢氧化铝沉淀消耗HCl的物质的量为(0.03L-0.01L)×1mol/L=0.02mol,由H2O+AlO2-+H+=Al(OH)3↓,可知氢氧化铝的物质的量为0.02mol,则氢氧化镁的质量为2.72g-0.02mol×78g/mol=0.02mol,由元素守恒可知,n(MgCl2)=n[Mg(OH)2]=0.02mol,n(AlCl3)=n[Al(OH)3]=0.02mol;
B点溶液中存在的溶质是NaCl,根据钠离子、氯离子守恒可知,n(NaOH)=n(NaCl)=n(HCl)+2n(MgCl2)+3n(AlCl3)=0.03L×1mol/L+0.02mol×2+0.02mol×3=0.13mol,
故答案为:0.02mol;0.02mol;0.13mol;
(3)C点溶液为MgCl2、AlCl3和NaCl混合液,由氯离子守恒可知,氯化钠中氯离子源于加入盐酸,根据钠离子守恒可知m(NaOH)=n(NaCl)=0.13mol,C点加入盐酸的体积为
| 0.13mol |
| 1mol/L |
故答案为:130.
点评:本题考查混合物有关计算,关键是明确每阶段发生的反应,再结合原子守恒来分析解答,(3)注意从化学式变化来分析,侧重考查学生分析计算能力,题目难度中等.

练习册系列答案
相关题目
下列各组指定原子序数的元素,不能形成AB型化合物的是( )
| A、7和8 | B、16和8 |
| C、12和8 | D、6和8 |
对1mol N2和1mol CO2进行比较,下列说法不正确的是( )
| A、分子数一定相同 |
| B、原子数一定不相同 |
| C、体积一定相同 |
| D、质量一定不相同 |
在实验室中,下列试剂不需要用棕色试剂瓶保存的是( )
| A、氯水 | B、硝酸银 |
| C、浓硝酸 | D、漂白粉 |
下列溶液中有关物质的量浓度关系不正确的( )
| A、pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) |
| B、0.1mol?L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(A2-)>c(H2A) |
| C、物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
| D、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) |