题目内容
电解NaCl溶液的装置如图所示,下列说法正确的是( )


| A、电解过程中NaCl溶液的pH下降 |
| B、溶液中Na+向铁电极方向移动 |
| C、通电一段时间后,可看到石墨电极附近溶液变红 |
| D、通电一段时间后,可看到试管中溶液变蓝 |
考点:电解原理
专题:电化学专题
分析:A、电解饱和食盐水,石墨做阳极,铁做阴极,溶液中氢离子在阴极得到电子生成氢气,溶液中氢氧根离子浓度增大;
B、电解过程中阳离子移向阴极;
C、石墨做阳极,溶液中氯离子失电子生成氯气,铁做阴极,溶液中氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大,酚酞变红色;
D、石墨电极是电解池阳极,溶液中氯离子失电子生成氯气,通入淀粉碘化钾溶液中氧化碘离子为碘单质.
B、电解过程中阳离子移向阴极;
C、石墨做阳极,溶液中氯离子失电子生成氯气,铁做阴极,溶液中氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大,酚酞变红色;
D、石墨电极是电解池阳极,溶液中氯离子失电子生成氯气,通入淀粉碘化钾溶液中氧化碘离子为碘单质.
解答:
解:A、电解饱和食盐水,石墨做阳极,铁做阴极,溶液中氢离子在阴极得到电子生成氢气,溶液中氢氧根离子浓度增大,溶液PH增大,故A错误;
B、电解过程中阳离子移向阴极,铁做阴极,溶液中Na+向铁电极方向移动,故B正确;
C、石墨做阳极,溶液中氯离子失电子生成氯气,铁做阴极,溶液中氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大,铁电极附近溶液中酚酞变红色,故C错误;
D、石墨电极是电解池阳极,溶液中氯离子失电子生成氯气,通入淀粉碘化钾溶液中氧化碘离子为碘单质,遇到碘单质变蓝,故D正确;
故选BD.
B、电解过程中阳离子移向阴极,铁做阴极,溶液中Na+向铁电极方向移动,故B正确;
C、石墨做阳极,溶液中氯离子失电子生成氯气,铁做阴极,溶液中氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大,铁电极附近溶液中酚酞变红色,故C错误;
D、石墨电极是电解池阳极,溶液中氯离子失电子生成氯气,通入淀粉碘化钾溶液中氧化碘离子为碘单质,遇到碘单质变蓝,故D正确;
故选BD.
点评:本题考查了电解原理的分析应用,主要是电极反应电极判断和溶液酸碱性的分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
能在透明溶液中大量共存的一组离子是( )
| A、Na+、NH4+、OH-、HCO3- |
| B、Mg2+、Ag+、NO3-、SiO32- |
| C、K+、Cu2+、Cl-、SO42- |
| D、H+、Fe3+、I-、ClO- |
甘油三油酸脂是一种典型的脂肪,当它在人体内代谢时发生下列反应C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)△H=-3.35×10 4 kJ?mol-1问如以高中男生平均每人每日耗能10125.3kJ,且以完全消耗这种脂肪来计算,每天需消耗甘油三油酸脂约( )
| A、1.2mol |
| B、0.6mol |
| C、0.3mol |
| D、0.15mol |
将一定量甘油[C3H5(OH)3]溶于甲苯中( ),混合液中氢元素质量分数为( )
),混合液中氢元素质量分数为( )
 ),混合液中氢元素质量分数为( )
),混合液中氢元素质量分数为( )| A、无法计算 | B、8.7% |
| C、17.4% | D、4.35% |
下列各组离子能大量共存的是( )
| A、NaClO水溶液中:Fe2+、Cl-、Ca2+、H+ |
| B、加入KSCN显红色的溶液:K+、Na+、I-、S2- |
| C、无色酸性溶液中:K+、CH3COO-、HCO3-、MnO4- |
| D、pH=2的溶液中:NH4+、Na+、Cl-、Cu2+ |
下列离子方程式书写正确的是( )
| A、Fe2O3溶于氢碘酸:Fe2O3+6HI=2Fe3++6I-+3H2O |
| B、Na2S溶液显碱性:S2-+2H2O=H2S+2OH- |
| C、CH3COOH与NaOH溶液反应:H++2OH-=H2O |
| D、AgNO3溶液中加入过量氨水:Ag++2NH3?H2O=Ag(NH3)2++2H2O |
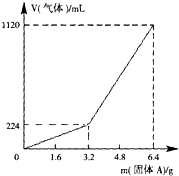 将一定量混合均匀的铁粉与硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A.将质量为m的固体A加入到300mL 2mol?L-1盐酸中使之完全溶解.测得室温下加入固体A的质量与收集到气体体积(已换算成标准状况)的关系如图15所示(假设所得氢硫酸溶液饱和前无硫化氢气体逸出).
将一定量混合均匀的铁粉与硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A.将质量为m的固体A加入到300mL 2mol?L-1盐酸中使之完全溶解.测得室温下加入固体A的质量与收集到气体体积(已换算成标准状况)的关系如图15所示(假设所得氢硫酸溶液饱和前无硫化氢气体逸出).