题目内容
铁是一种过渡元素,金属铁是最常用的金属.请回答下列各题:
(1)生铁中含有一种铁碳化合物(Fe3C),在足量的空气中高温煅烧,生成有磁性的固体和能使澄清石灰水变浑浊的气体,该反应的化学方程式为 .上述反应生成的磁性固体能溶于过量盐酸,该反应的离子方程式为 .
(2)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化.已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为 .
(3)硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制绿矾.利用烧渣制绿矾的过程如下:

①烧渣溶于稀H2SO4过程中,有单质硫生成,写出该反应的离子方程式(只写生成S的反应式,其他反应无需写出) .
②向溶液X中加入足量铁屑的目的是 .
③可用硫酸酸化的 KMnO4溶液通过滴定法测定绿矾产品中FeSO4含量,滴定时发生反应的离子方程式为 .
(4)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36.室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH=3时,通过计算说明Fe3+是否沉淀完全 .
(提示:当某离子浓度小于1.0×10-5 mol?L-1时可以认为该离子沉淀完全了)
(1)生铁中含有一种铁碳化合物(Fe3C),在足量的空气中高温煅烧,生成有磁性的固体和能使澄清石灰水变浑浊的气体,该反应的化学方程式为
(2)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化.已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为
(3)硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制绿矾.利用烧渣制绿矾的过程如下:

①烧渣溶于稀H2SO4过程中,有单质硫生成,写出该反应的离子方程式(只写生成S的反应式,其他反应无需写出)
②向溶液X中加入足量铁屑的目的是
③可用硫酸酸化的 KMnO4溶液通过滴定法测定绿矾产品中FeSO4含量,滴定时发生反应的离子方程式为
(4)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36.室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH=3时,通过计算说明Fe3+是否沉淀完全
(提示:当某离子浓度小于1.0×10-5 mol?L-1时可以认为该离子沉淀完全了)
考点:铁盐和亚铁盐的相互转变
专题:几种重要的金属及其化合物
分析:(1)Fe3C在足量的空气中高温煅烧生成四氧化三铁和二氧化碳;磁性固体能溶于过量稀硝酸发生氧化还原反应生成硝酸铁、NO和水;
(2)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化,由总反应(2SO2+O2+2H2O=2H2SO4)减去4Fe2++O2+4H+=4Fe3++2H2O即可;
(3)①Fe2O3和FeS均可以和稀硫酸之间反应分别生成硫酸铁、硫化氢,二者之间会发生化学反应;
②金属铁可以和铁离子之间反应生成亚铁离子;
③高锰酸根离子具有氧化性,能将亚铁离子氧化为铁离子.
(4)溶液中c(H+)=10-3,c(OH-)=10-11 ,代入Ksp=1.1×10-36=[c(OH-)]3×c(Fe3+)求算.
(2)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化,由总反应(2SO2+O2+2H2O=2H2SO4)减去4Fe2++O2+4H+=4Fe3++2H2O即可;
(3)①Fe2O3和FeS均可以和稀硫酸之间反应分别生成硫酸铁、硫化氢,二者之间会发生化学反应;
②金属铁可以和铁离子之间反应生成亚铁离子;
③高锰酸根离子具有氧化性,能将亚铁离子氧化为铁离子.
(4)溶液中c(H+)=10-3,c(OH-)=10-11 ,代入Ksp=1.1×10-36=[c(OH-)]3×c(Fe3+)求算.
解答:
解:(1)Fe3C在足量的空气中高温煅烧生成四氧化三铁和二氧化碳,反应为Fe3C+3O2
Fe3O4+CO2;磁性固体能溶于过量稀硝酸发生氧化还原反应生成硝酸铁、NO和水,离子反应为3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,
故答案为:Fe3C+3O2
Fe3O4+CO2;3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O;
(2)由总反应(2SO2+O2+2H2O=2H2SO4)减去4Fe2++O2+4H+=4Fe3++2H2O可得到离子反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(3)①Fe2O3可以和稀硫酸之间反应生成硫酸铁,FeS可以和稀硫酸之间反应生成硫化氢,铁离子具有氧化性,硫化氢具有还原性,二者之间会发生化学反应:2Fe3++H2S=2Fe2++S↓+2H+,会产生硫单质,故答案为:2Fe3++H2S=2Fe2++S↓+2H+;
②向溶液硫酸铁中加入足量铁屑,金属铁可以和铁离子之间反应生成亚铁离子,以制备纯净的绿矾晶体,故答案为:使Fe3+完全转化为Fe2+,以制备纯净的绿矾晶体;
③高锰酸根离子具有氧化性,能将亚铁离子氧化为铁离子,实质是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(4)溶液pH为3时,溶液中c(H+)=10-3,则c(OH-)=10-11 ,Ksp=1.1×10-36=[c(OH-)]3×c(Fe3+),c(Fe3+)=1.1×10-36/10-33=1.1×10-3(mol/L)>10-5 mol?L-1,故答案为:c(Fe3+)=1.1×10-3(mol/L)>10-5 mol?L-1故Fe3+没有沉淀完全.
| ||
故答案为:Fe3C+3O2
| ||
(2)由总反应(2SO2+O2+2H2O=2H2SO4)减去4Fe2++O2+4H+=4Fe3++2H2O可得到离子反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(3)①Fe2O3可以和稀硫酸之间反应生成硫酸铁,FeS可以和稀硫酸之间反应生成硫化氢,铁离子具有氧化性,硫化氢具有还原性,二者之间会发生化学反应:2Fe3++H2S=2Fe2++S↓+2H+,会产生硫单质,故答案为:2Fe3++H2S=2Fe2++S↓+2H+;
②向溶液硫酸铁中加入足量铁屑,金属铁可以和铁离子之间反应生成亚铁离子,以制备纯净的绿矾晶体,故答案为:使Fe3+完全转化为Fe2+,以制备纯净的绿矾晶体;
③高锰酸根离子具有氧化性,能将亚铁离子氧化为铁离子,实质是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(4)溶液pH为3时,溶液中c(H+)=10-3,则c(OH-)=10-11 ,Ksp=1.1×10-36=[c(OH-)]3×c(Fe3+),c(Fe3+)=1.1×10-36/10-33=1.1×10-3(mol/L)>10-5 mol?L-1,故答案为:c(Fe3+)=1.1×10-3(mol/L)>10-5 mol?L-1故Fe3+没有沉淀完全.
点评:本题考查较综合,涉及氧化还原反应的计算、离子反应和化学反应方程式的书写等,综合性较强,侧重分析能力与计算能力的综合考查,题目难度中等.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
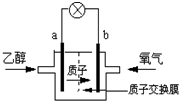 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )| A、b极为电池的负极 |
| B、设每个电子所带电量为q库仑,则1mol乙醇被氧化产生12NAq库仑的电量 |
| C、电池工作时电流由a极沿导线经灯泡再到b极 |
| D、电池正极的电极反应为:O2+4e-+2H2O=4OH- |
下列有关说法不正确的是( )
| A、实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| B、为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
| C、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ?mol-1则水电离的热化学方程式为:H2O(l)?H+(aq)+OH-(aq)△H=+57.3 kJ?mol-1 |
| D、生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe-2e-=Fe2+ |
下列各元素一定属于主族元素的是( )
| A、X元素的次外层上有18个电子 |
| B、Y元素的最外层上有2个电子 |
| C、Z元素形成的单核阳离子,具有稀有气体元素的核外电子排布 |
| D、R元素形成的单核阴离子,具有稀有气体元素的核外电子排布 |