题目内容
14.下列说法正确的是( )| A. | 电解法精炼铜是,以粗铜作阴极,精铜作阳极 | |
| B. | 加热0.1mol/L的Na2CO3溶液,CO32-的水解程度和溶液的pH均增大 | |
| C. | 1L 1mol/L的NaClO溶液中含有ClO-的数目为6.02×1023 | |
| D. | 相同条件下,溶液中Fe2+、Cu2+、Zn2+的氧化性依次减弱 |
分析 A.电镀法精炼铜时,粗铜为阳极,精铜为阴极;
B.加热促进水解,溶液碱性增强;
C.NaClO溶液中含有ClO-能发生水解;
D.相同条件下,溶液中Fe2+、Cu2+、Zn2+的氧化性为Cu2+、Fe2+、Zn2+.
解答 解:A.阳极材料是粗铜,阳极上失电子变成离子进入溶液,Cu-2e-=Cu2+,精铜作阴极,故A错误;
B.碳酸钠溶液中碳酸根离子水解显碱性,加热0.1mol/L的Na2CO3溶液,CO32-的水解程度和溶液的pH均增大,故B正确;
C.NaClO溶液中含有ClO-能发生水解,1L 1mol/L的NaClO溶液中含有ClO-的数目小于6.02×1023 ,故C错误;
D.相同条件下,溶液中Fe2+、Cu2+、Zn2+的氧化性减弱的顺序为:Cu2+、Fe2+、Zn2+,故D错误;
故选B.
点评 本题考查了电解精炼、盐类水解影响因素、离子性质等知识点,掌握基础是解题关键,题目难度中等.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 60g C2H4O2所含共用电子对数目为7NA | |
| B. | 1L 0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 1mol甲基或氨基所含电子数均为9NA | |
| D. | 标准状况下,22.4L乙醇的分子数为NA |
19.下列各项与化学平衡移动原理无关的是( )
| A. | 收集Cl2用排饱和食盐水的方法 | |
| B. | 加催化剂,使SO2和O2 在一定条件下转化为SO3 | |
| C. | 可用浓氨水和NaOH(s)快速制取氨气 | |
| D. | 加压条件下有利于N2和H2反应生成NH3 |
6.下列有机物中,能以任意比与水互 溶的是( )
| A. | 苯 | B. | 乙烷 | C. | 酒精 | D. | 汽油 |

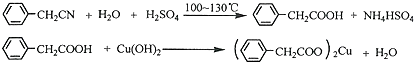
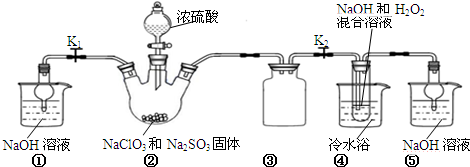
 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: