题目内容
12.下列事实与盐类水解无关的是( )| A. | 氯化铝溶液蒸干后灼烧得不到无水氯化铝 | |
| B. | 氯化铁溶液常用作制印刷电路板的腐蚀剂 | |
| C. | 常用热的纯碱溶液除去油污 | |
| D. | 长期施用硫酸铵易使土壤酸化 |
分析 A.氯化铝水解生成氢氧化铝和HCl;
B.氯化铁溶液与铜反应生成氯化亚铁和氯化铜;
C.油脂属于酯类,在碱性条件下发生水解;
D.铵根离子水解显酸性.
解答 解:A.氯化铝水解生成氢氧化铝和HCl,加热HCl挥发促进水解,最终得不到无水氯化铝,故A不选;
B.氯化铁溶液与铜反应生成氯化亚铁和氯化铜,发生了氧化还原反应,与盐类水解无关,故B选;
C.纯碱为Na2CO3,在溶液中水解显碱性,加热碱性增强,而油脂属于酯类,在碱性条件下发生水解,故纯碱能去油污,故C不选;
D.铵根离子在溶液中会水解显酸性,所以长期施用硫酸铵易使土壤酸化,故D不选.
故选B.
点评 本题考查盐类水解的应用,侧重于化学知识的综合运用的考查,注意把握盐类水解的原理,题目难度不大.

练习册系列答案
相关题目
20.下列实验或生产能达到目的是( )
| A. | 电解熔融的AlCl3生产铝单质 | |
| B. | 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 | |
| C. | 用Ba(OH)2溶液可鉴别NaCl、AlCl3、NH4Cl、Na2SO4四种溶液 | |
| D. | 用分液漏斗从食醋中分离出乙酸 |
7.下列各组澄清溶液中离子能大量共存,且加入(或滴入)X试剂后发生反应的离子方 程式书写正确的是( )
| 选项 | 离子组 | X试剂 | 离子方程式 |
| A | K+、Na+、ClO-、SO42- | 少量SO2 | SO2+ClO-+H2O═SO42-+Cl-+2H+ |
| B | NH4+、Fe3+、Br-、SO42- | 过量H2S | 2Fe3++H2S═2Fe2++S↓+2H+ |
| C | NH4+、Na+、Fe3+、[Al(OH)4]- | 过量铜粉 | 2Fe3++Cu═2Fe2++Cu2+ |
| D | K+、Na+、HCO3-、Al3+ | 少量HCl | H++HCO3-═CO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |
17.下列离子在溶液中能大量共存的是( )
| A. | H+、AlO2-、CO32- | B. | K+、Ba2+、SO42- | C. | NH4+、OH-、NO3- | D. | Fe3+、NO3-、Cl- |
4.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.8gNH4+中含有的电子数为NA | |
| B. | 标准状况下,足量Na2O2与22.4LCO2气体充分反应,转移电子数为2NA | |
| C. | 2molSO2和1molO2在一定条件下充分反应,所得混合气体的分子数等于2NA | |
| D. | 298K时,1.0LpH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
1.下列叙述中错误的是( )
| A. | 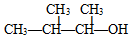 的命名为:3-甲基-2-丁醇 的命名为:3-甲基-2-丁醇 | |
| B. | 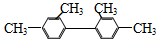 分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面 | |
| C. | 羟基的电子式是 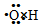 | |
| D. | 软脂酸和油酸互为同系物 |
12.C和H2在生产、生活、科技中是重要的燃料.
①2C(s)+O2(g)═2CO(g)△H1=-220kJ/mol
②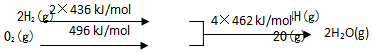
下列推断正确的是( )
①2C(s)+O2(g)═2CO(g)△H1=-220kJ/mol
②

下列推断正确的是( )
| A. | C(s)的燃烧热110 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H1=+480 kJ/mol | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H1=+130 kJ/mol | |
| D. | 欲分解2 mol H2O(l),至少需要提供4×462 kJ 的热量 |
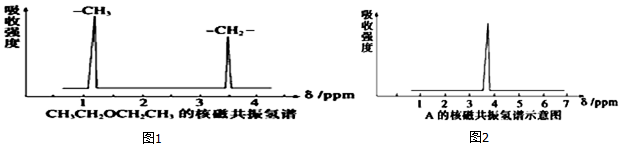
 ,其核磁共振氢谱中有2个信号(参见图1).
,其核磁共振氢谱中有2个信号(参见图1).