题目内容
9.在下列化合物 ①H2O、②H2O2、③Ba(OH)2、④Na2O2、⑤MgCl2中,(1)只由离子键构成的化合物是⑤(填序号,下同)
(2)由离子键和非极性键构成的化合物是④
(3)由极性键和非极性键构成的化合物是②.
分析 大多非金属元素之间形成的键是共价键,活泼金属和活泼的非金属之间形成的键大多是离子键,含有离子键的化合物为离子化合物,共价化合物只含共价键,成键元素相同的共价键是非极性键,成键元素不同的共价键是极性键.
解答 解:大多非金属元素之间形成的键是共价键,活泼金属和活泼的非金属之间形成的键大多是离子键,含有离子键的化合物为离子化合物,共价化合物只含共价键,
(1)仅由离子键构成的化合物有MgCl2,故答案为:⑤;
(2)由离子键和非极性键构成的化合物是④Na2O2,故答案为:④;
(3)由极性键和非极性键构成的化合物是②H2O2,故答案为:②;
点评 本题考查化学键知识,为高频考点,侧重于基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
20.一定温度时,向2.0L恒容密闭容器中充入2molSO2和1molO2,发生反应:2SO2(g)+O2(g)?2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
| A. | 反应在前t1s的平均速率v(O2)=0.4/t1mol•L-1•s-1 | |
| B. | 保持其他条件不变,体积压缩到1.0L,平衡常数将增大 | |
| C. | 保持温度不变,向该容器中再充入0.3 molSO2、0.1molO2和0.2molSO3,则此时V正>V逆 | |
| D. | 相同温度下,起始时向容器中充入4mol SO3,达到平衡时,SO3的转化率大于10% |
17.氯碱工业是最基本的化学工业之一,它的产品除应用于化学工业本身外,还广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业.考虑到生产实际经济效益吸收氯碱工业的尾气氯气最好采用( )
| A. | 浓NaOH溶液 | B. | 饱和食盐水 | C. | 石灰乳 | D. | 浓硫酸 |
4.已知在一定条件下,二个氨基酸分子之间失去一分子水,缩合生成“二肽”.现将甘氨酸[CH2(NH2)-COOH]和丙氨酸[CH3-CH(NH2)-COOH]组成的混合物,在一定条件下发生缩合反应,生成的“二肽”可能有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
14.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6gFe和足量的盐酸完全反应失去电子数为0.3 NA | |
| B. | 1.0mol•L的NaCl 溶液中Na+数为NA | |
| C. | 16gCH4所含的电子数为10NA | |
| D. | 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
1.实验室制Cl2的反应如下:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,下列有关该反应的说法正确的是( )
| A. | MnO2是还原剂 | B. | HCl被氧化 | ||
| C. | MnO2发生氧化反应 | D. | 每反应4molHCl转移4mol电子 |
18.下列各醇,能发生催化氧化的是( )
| A. | 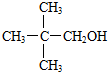 | B. |  | C. | 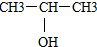 | D. | 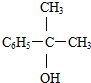 |
19.下列分离或提纯有机物的方法正确的是( )
| 选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
| A | 乙烷 | 乙烯 | 酸性KMnO4溶液,洗气 |
| B | MgCl2溶液 | FeCl3 | MgO,过滤 |
| C | HCl气体 | Cl2 | 饱和食盐水,洗气 |
| D | 乙醇 | 水 | 生石灰,过滤 |
| A. | A | B. | B | C. | C | D. | D |