题目内容
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是( )
| A、pH大于7的溶液:Na+、Ba2+、SO32-、ClO- |
| B、含有0.1 mol?L-1 Fe(NO3)2的溶液:H+、Mg2+、SCN-、Cl- |
| C、使酚酞试液变红色的溶液:Na+、Ba2+、I-、Cl- |
| D、由水电离产生的c(H+)=10-13mol?L-1的溶液:NH4+、SO42-、NO3-、Cl- |
考点:离子共存问题
专题:
分析:A.次氯酸根离子能够氧化亚硫酸根离子,亚硫酸根离子与钡离子反应生成亚硫酸钡沉淀;
B.硝酸根离子在酸性条件下能够将亚铁离子氧化成铁离子,铁离子能够与硫氰根离子反应生成硫氰化铁;
C.使酚酞试液变红色的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
D.水电离产生的c(H+)=10-13mol?L-1的溶液中存在大量氢离子或氢氧根离子,铵根离子与氢氧根离子反应.
B.硝酸根离子在酸性条件下能够将亚铁离子氧化成铁离子,铁离子能够与硫氰根离子反应生成硫氰化铁;
C.使酚酞试液变红色的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
D.水电离产生的c(H+)=10-13mol?L-1的溶液中存在大量氢离子或氢氧根离子,铵根离子与氢氧根离子反应.
解答:
解:A.pH大于7的溶液为碱性溶液,溶液中存在大量氢氧根离子,Ba2+、SO32-之间反应生成亚硫酸钡,SO32-、ClO-之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.H+大量存在条件下,NO3-具有强氧化性,能够氧化Fe2+,SCN-与氧化生成的铁离子反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.使酚酞试液变红色的溶液为碱性溶液,溶液中存在大量氢氧根离子,Na+、Ba2+、I-、Cl-之间不发生反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.水电离产生的c(H+)=10-13mol?L-1的溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,若为碱性溶液,NH4+能够与氢氧根离子反应,在溶液中不能大量共存,故D错误;
故选C.
B.H+大量存在条件下,NO3-具有强氧化性,能够氧化Fe2+,SCN-与氧化生成的铁离子反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.使酚酞试液变红色的溶液为碱性溶液,溶液中存在大量氢氧根离子,Na+、Ba2+、I-、Cl-之间不发生反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.水电离产生的c(H+)=10-13mol?L-1的溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,若为碱性溶液,NH4+能够与氢氧根离子反应,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存的判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还要明确题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的H+或OH-;是“可能”共存,还是“一定”共存等.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
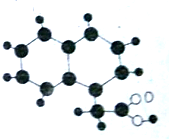 2009年《化学教育》期刊封面刊载如图所示的有机物M(只含C、H、O)的球棍模型图.不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键.下列有关M的推断正确的是( )
2009年《化学教育》期刊封面刊载如图所示的有机物M(只含C、H、O)的球棍模型图.不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键.下列有关M的推断正确的是( )| A、M的分子式为C12H12O2 |
| B、M与足量氢气在一定条件下反应的产物的环上一氯代物有7种 |
| C、M能发生中和反应、取代反应 |
| D、一个M分子最多有11个原子共面 |
下列各元素原子排列中,按其半径逐渐增大,电负性逐渐减小顺序排列正确的是( )
| A、K、Na、Li |
| B、F、O、S |
| C、As、P、N |
| D、C、N、O |
下列离子方程式与所述事实相符且正确的是( )
| A、向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| B、用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、用稀硝酸清洗银镜反应实验后的试管:3Ag+4H++NO3-=3Ag++NO↑+2H2O |
| D、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |
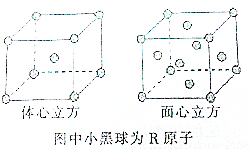 X、Y、Z、W、R是原子序数依次增大的前四周期元素.X的单质在Y2中燃烧可生成XY和XY2两种气体;Z的单质在Y2中燃烧的产物ZY2可使品红溶液褪色;W的单质是黄绿色的有毒气体;R3+离子的3d轨道半充满.
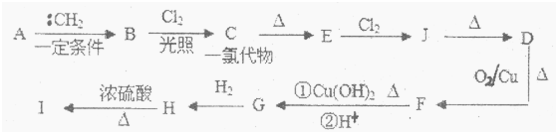
X、Y、Z、W、R是原子序数依次增大的前四周期元素.X的单质在Y2中燃烧可生成XY和XY2两种气体;Z的单质在Y2中燃烧的产物ZY2可使品红溶液褪色;W的单质是黄绿色的有毒气体;R3+离子的3d轨道半充满.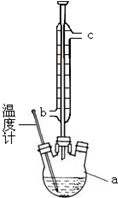 阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:
阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为: