题目内容
20.如图装置可实现电解CuCl2溶液,c、d均为石墨.下列说法正确的是( )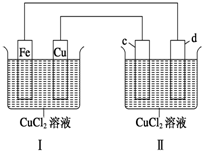
| A. | Ⅰ和Ⅱ无外加电源,都是原电池 | |
| B. | 铁为负极,d为阴极,两个电极上都发生还原反应 | |
| C. | Ⅰ中铜电极Ⅱ中c电极上有铜析出 | |
| D. | Ⅰ是原电池,Ⅱ是电解池 |
分析 装置Ⅰ铁与铜活泼性不同,浸在电解质氯化铜溶液中,存在铁与氯化铜生成氯化亚铁和铜的自发的氧化还原反应,符合原电池条件,为原电池,铁性质活泼为原电池负极,失去电子发生氧化反应生成二价铁离子,铜为正极,溶液中铜离子在铜极得到电子发生还原反应生成铜;
装置Ⅱ用惰性电极电解氯化铜溶液,用装置Ⅰ提供电源,C与装置Ⅰ正极相连,为电解池阳极,氯离子在c极失去电子发生氧化反应生成氯气,d为阴极,铜离子在d电极得到电子发生还原反应生成铜,据此解答.
解答 解:A.装置Ⅰ铁与铜活泼性不同,浸在电解质氯化铜溶液中,存在铁与氯化铜生成氯化亚铁和铜的自发的氧化还原反应,符合原电池条件,为原电池,装置Ⅱ用惰性电极电解氯化铜溶液,用装置Ⅰ提供电源,故A错误;
B.铁性质活泼为原电池负极,发生氧化反应,d为电解池阴极发生还原反应,故B错误;
C.Ⅰ中铜电极为原电池正极,铜离子在正极析出;Ⅱ中c电极为阳极,氯离子失去电子生成氯气,不会析出铜,故C错误;
D.装置Ⅰ铁与铜活泼性不同,浸在电解质氯化铜溶液中,存在铁与氯化铜生成氯化亚铁和铜的自发的氧化还原反应,符合原电池条件,为原电池,装置Ⅱ用惰性电极电解氯化铜溶液,用装置Ⅰ提供电源,故D正确;
故选:D.
点评 本题为电化学题,考查了电解池、原电池工作原理,准确判断装置类型及电极、电极上发生的反应是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列有关同分异构体数目的说法不正确的是( )

| A. | 甲苯中一个氢原子被氯原子取代,有机产物有3种 | |
| B. | 苯环上的一氯取代物的同分异构体有2种 | |
| C. | C5H12的一氯代物有8种 | |
| D. | C7H8O含苯环的同分异构体有5种 |
11.下列关于乙醇的物理性质的叙述中,错误的是( )
| A. | 能与水任意比例互溶 | B. | 可溶解多种无机物和有机物 | ||
| C. | 密度比水小 | D. | 沸点比水高 |
8.下列说法正确的是( )
| A. | P4和NO2都是共价化合物 | B. | CCl4和NH3分子中都含有极性键 | ||
| C. | CaO和SiO2都是离子化合物 | D. | Na2O2是离子化合物,只含有离子键 |
15.下列各组中属于同位素关系的是( )
| A. | 红磷与白磷 | B. | D2与H2 | C. | 40K与39K | D. | 40K与40Ca |
5.下列化学用语使用正确的是( )
| A. | 葡萄糖、淀粉的最简式都是CH2O | B. | 醋酸钠的分子式:CH3COONa | ||
| C. | CH4的电子式是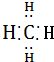 | D. | 丙烷分子的球棍模型是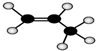 |
18.某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3min
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)0.1mol/(L•min).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液:
A.蒸馏水B.NaCl溶液C.Na2CO3 溶液D.CuSO4溶液你认为可行的是(填编号)AB.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)0.1mol/(L•min).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液:
A.蒸馏水B.NaCl溶液C.Na2CO3 溶液D.CuSO4溶液你认为可行的是(填编号)AB.
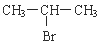 ③
③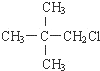 ④
④