题目内容
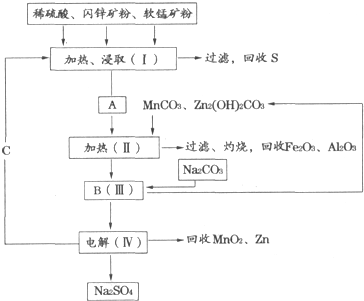
根据要求完成下列实验过程(a、b为弹簧夹,加热及固定装置已略去).

(1)验证SO2的氧化性、还原性和酸性氧化物的通性.
①连接仪器、 、加药品后,打开a、关闭b,然后滴入浓硫酸.
②装置A中发生的化学方程式是 .
③验证SO2的氧化性的实验现象是 .
④BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入表相应位置.写出其中SO2显示还原性生成沉淀的离子方程式: .
(2)验证碳、硅非金属性的相对强弱.
①在(1)①操作后打开b,关闭a.
②NaHCO3饱和溶液中发生的离子反应方程式为 .
③实验过程中,C中出现白色沉淀.甲同学认为不能由此说明碳的非金属性比硅强,需增加一个实验装置才能获得可靠实验结论,其改进方法为 .

(1)验证SO2的氧化性、还原性和酸性氧化物的通性.
①连接仪器、
②装置A中发生的化学方程式是
③验证SO2的氧化性的实验现象是
④BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入表相应位置.写出其中SO2显示还原性生成沉淀的离子方程式:
| 滴加的溶液 | 氨水 | 氯水 |
| 沉淀的化学式 |
①在(1)①操作后打开b,关闭a.
②NaHCO3饱和溶液中发生的离子反应方程式为
③实验过程中,C中出现白色沉淀.甲同学认为不能由此说明碳的非金属性比硅强,需增加一个实验装置才能获得可靠实验结论,其改进方法为
考点:性质实验方案的设计
专题:
分析:(1)①反应生成气体,在加入药品之前需要检验装置的气密性;
②装置A的作用是制取二氧化硫,浓硫酸与亚硫酸钠反应生成二氧化硫;
③二氧化硫能把硫化氢氧化成硫单质,生成淡黄色沉淀;
④二氧化硫通入BaCl2溶液中,滴加氯水溶液,氯水中有氯气分子,二氧化硫能把氯气还原成盐酸,自身被氧化成硫酸,硫酸根离子和钡离子反应生成硫酸钡白色沉淀;
(2)②A中产生的二氧化硫气体通入B中反应生成亚硫酸钠和二氧化碳;
③从B中出来的二氧化硫气体必须除干净,产生白色沉淀才能说明碳的非金属性比硅强,在B、C间加一个除二氧化硫的装置.
②装置A的作用是制取二氧化硫,浓硫酸与亚硫酸钠反应生成二氧化硫;
③二氧化硫能把硫化氢氧化成硫单质,生成淡黄色沉淀;
④二氧化硫通入BaCl2溶液中,滴加氯水溶液,氯水中有氯气分子,二氧化硫能把氯气还原成盐酸,自身被氧化成硫酸,硫酸根离子和钡离子反应生成硫酸钡白色沉淀;
(2)②A中产生的二氧化硫气体通入B中反应生成亚硫酸钠和二氧化碳;
③从B中出来的二氧化硫气体必须除干净,产生白色沉淀才能说明碳的非金属性比硅强,在B、C间加一个除二氧化硫的装置.
解答:
解:(1)①装置A中反应制备气体,在加入药品之前需要检验装置的气密性,
故答案为:检验装置的气密性;
②装置A的作用是制取二氧化硫,浓硫酸与亚硫酸钠反应生成二氧化硫,反应方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,
故答案为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
③二氧化硫中硫元素的化合价是+4价,有氧化性,二氧化硫气体与H2S溶液常温下反应,生成黄色固体硫(单质)和水,2H2S+SO2=3S↓+2H2O,此反应可以证明二氧化硫的氧化性,故答案为:H2S溶液中有淡黄色浑浊出现;
④二氧化硫通入BaCl2溶液中,滴加氯水溶液,氯水中有氯气分子,二氧化硫能把氯气还原成盐酸,自身被氧化成硫酸,硫酸根离子和钡离子反应生成硫酸钡白色沉淀,总反应为:Ba2++SO2+Cl2+2H2O═BaSO4↓+4H++2Cl-;故答案为:Ba2++SO2+Cl2+2H2O═BaSO4↓+4H++2Cl-;
(2)②A中产生的二氧化硫气体通入B中反应生成亚硫酸钠和二氧化碳,反应方程式为SO2+2HCO3-=2SO32-+H2O+2CO2,故答案为:SO2+2HCO3-=2SO32-+H2O+2CO2;
③从B中出来的二氧化硫气体必须除干净,产生白色沉淀才能说明碳的非金属性比硅强,在B、C之间增加一个装有酸性高锰酸钾溶液的洗气瓶,故答案为:在B、C之间增加一个装有酸性高锰酸钾溶液的洗气瓶.
故答案为:检验装置的气密性;
②装置A的作用是制取二氧化硫,浓硫酸与亚硫酸钠反应生成二氧化硫,反应方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,
故答案为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
③二氧化硫中硫元素的化合价是+4价,有氧化性,二氧化硫气体与H2S溶液常温下反应,生成黄色固体硫(单质)和水,2H2S+SO2=3S↓+2H2O,此反应可以证明二氧化硫的氧化性,故答案为:H2S溶液中有淡黄色浑浊出现;
④二氧化硫通入BaCl2溶液中,滴加氯水溶液,氯水中有氯气分子,二氧化硫能把氯气还原成盐酸,自身被氧化成硫酸,硫酸根离子和钡离子反应生成硫酸钡白色沉淀,总反应为:Ba2++SO2+Cl2+2H2O═BaSO4↓+4H++2Cl-;故答案为:Ba2++SO2+Cl2+2H2O═BaSO4↓+4H++2Cl-;
(2)②A中产生的二氧化硫气体通入B中反应生成亚硫酸钠和二氧化碳,反应方程式为SO2+2HCO3-=2SO32-+H2O+2CO2,故答案为:SO2+2HCO3-=2SO32-+H2O+2CO2;
③从B中出来的二氧化硫气体必须除干净,产生白色沉淀才能说明碳的非金属性比硅强,在B、C之间增加一个装有酸性高锰酸钾溶液的洗气瓶,故答案为:在B、C之间增加一个装有酸性高锰酸钾溶液的洗气瓶.
点评:本题考查实验方案的设计,涉及物质性质、对装置的理解等,难度不大,理解实验原理是解题的关键,注意基础知识的理解掌握.

练习册系列答案
相关题目
将CH4和C2H4的混合气体15g通入盛有足量溴水的容器中,溴水的质量增加了7g,则混合气体中CH4和C2H4的体积比为( )
| A、1:2 | B、2:1 |
| C、3:2 | D、2:3 |
M、X、Y、Z、W为五种短周期元素,原子序数依次递增,X、Y、Z是同周期元素,且最外层电子数之和为15,X与Z可形成气体分子XZ2,Y与M形成的气态化合物密度在相同状况下是氢气的8.5倍,W的质子数是M、X、Y、Z四种元素质子数之和的一半.下列说法正确的是( )
| A、原子半径:X>Z>Y>X>M |
| B、XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C、由X、Y、Z、M四种元素形成的化合物不能含有有离子键 |
| D、由X元素形成的某种单质能导电,可以做电极 |
将4.28gNa、Na2O、Na2O2的混合物与足量水反应,在标准状况下得到672mL混合气体,该混合气体在放电条件下恰好完全反应,则原混合物中各物质的物质的量之比为( )
| A、1:1:1 |
| B、1:1:2 |
| C、1:2:1 |
| D、4:3:2 |
下列物质中,含有自由移动Cl-的是( )
| A、KClO3溶液 |
| B、液态HCl |
| C、熔融NaCl |
| D、KCl晶体 |