题目内容
6.下列有关氧气和二氧化碳的说法不正确的是( )| A. | 自然界中的氧气和二氧化碳通过光合作用与呼吸作用可以相互转化 | |
| B. | 实验室制氧气和二氧化碳都可通过分解反应制得 | |
| C. | 氧气和二氧化碳都可以用向上排空气法收集 | |
| D. | 一般情况下,氧气能支持燃烧,二氧化碳不能支持燃烧 |
分析 A.植物光合作用吸收二氧化碳,呼出氧气;
B.高锰酸钾受热分解生成氧气,碳酸钙与盐酸反应生成二氧化碳、氯化钙和水,结合分解反应概念判断;
C.可以用向上排空气法收集的气体密度大于空气密度;
D.根据物质的化学性质来分析.
解答 解:A.在光合作用中,二氧化碳是原料,氧气时产物;在呼吸作用中,氧气是原料,二氧化碳是产物,故A正确;
B.高锰酸钾受热分解生成氧气,属于分解反应,碳酸钙与盐酸反应生成二氧化碳、氯化钙和水,属于复分解反应,不是分解反应,故B错误;
C.二氧化碳、氧气密度大于空气,可以用向上排空气法收集,故C正确;
D.氧气具有助燃性,二氧化碳既不能燃烧也不能支持燃烧,故D正确;
故选B.
点评 本题考查了氧气和二氧化碳的循环、结构以及性质,熟悉相关物质的性质是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
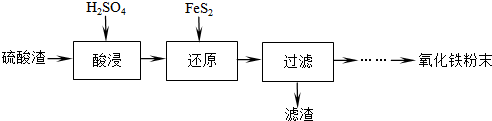
(1)“酸浸”中硫酸要适当过量,目的是提高铁的浸出率,抑制Fe3+的水解.
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO42-+16H+.
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量.实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定.有关反应的化学方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-;
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
滴定时,K2Cr2O7标准溶液应盛放在酸式滴定管中(填“酸式”、“碱式”);若不加HgCl2,则测定的Fe3+量偏高(填“偏高”、“偏低”或“不变”).
(4)①可选用KSCN(填试剂)检验滤液中含有Fe3+,产生Fe3+的原因是4Fe2++O2+4H+=4Fe3++2H2O(用离子方程式表示).
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
实验可选用的试剂有:稀硝酸、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体.请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:向溶液中加入过量的酸性高锰酸钾溶液,搅拌.
b.沉淀:滴加NaOH溶液,调节溶液为pH为3.2~3.8.
c.分离,洗涤.
d.烘干,研磨.

(1)“酸浸”中硫酸要适当过量,目的是提高铁的浸出率,抑制Fe3+的水解.
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO42-+16H+.
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量.实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定.有关反应的化学方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-;
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
滴定时,K2Cr2O7标准溶液应盛放在酸式滴定管中(填“酸式”、“碱式”);若不加HgCl2,则测定的Fe3+量偏高(填“偏高”、“偏低”或“不变”).
(4)①可选用KSCN(填试剂)检验滤液中含有Fe3+,产生Fe3+的原因是4Fe2++O2+4H+=4Fe3++2H2O(用离子方程式表示).
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
a.氧化:向溶液中加入过量的酸性高锰酸钾溶液,搅拌.
b.沉淀:滴加NaOH溶液,调节溶液为pH为3.2~3.8.
c.分离,洗涤.
d.烘干,研磨.
14. 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下:
熔融氧化3MnO2+KClO3+6KOH$\frac{\underline{\;熔融\;}}{\;}$3K2MnO4+KCl+3H2O
加酸歧化3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
相关物质的溶解度(293K)见下表:
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd.(填字母)
a.表面皿 b.蒸发皿 c.铁坩埚 d.泥三角
(2)加酸时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
(3)采用电解法也可以实现K2MnO4的转化,2K2MnO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率.
(4)草酸钠滴定法分析高锰酸钾纯度步骤如下:
Ⅰ称取0.80g 左右的高锰酸钾产品,配成50mL溶液.
Ⅱ准确称取0.2014g左右已烘干的Na2C2O4,置于锥形瓶中,加入少量蒸馏水使其溶解,再加入少量硫酸酸化.
Ⅲ将瓶中溶液加热到75~80℃,趁热用Ⅰ中配制的高锰酸钾溶液滴定至终点.记录消耗高锰酸钾溶液的体积,计算得出产品纯度.
①滴定过程中反应的离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
②达到滴定终点的标志为锥形瓶中溶液突变为浅红色且半分钟内不褪色.
③加热温度大于90℃,部分草酸发生分解,会导致测得产品纯度偏高.(填“偏高”、“偏低”或“无影响”)
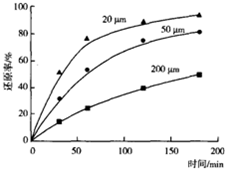
④将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如右图,其原因可能为生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快.
 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下:熔融氧化3MnO2+KClO3+6KOH$\frac{\underline{\;熔融\;}}{\;}$3K2MnO4+KCl+3H2O
加酸歧化3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
相关物质的溶解度(293K)见下表:
| K2CO3 | KHCO3 | K2SO4 | KMnO4 | |
| 溶解度/g | 111 | 33.7 | 11.1 | 6.34 |
a.表面皿 b.蒸发皿 c.铁坩埚 d.泥三角
(2)加酸时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
(3)采用电解法也可以实现K2MnO4的转化,2K2MnO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率.
(4)草酸钠滴定法分析高锰酸钾纯度步骤如下:
Ⅰ称取0.80g 左右的高锰酸钾产品,配成50mL溶液.
Ⅱ准确称取0.2014g左右已烘干的Na2C2O4,置于锥形瓶中,加入少量蒸馏水使其溶解,再加入少量硫酸酸化.
Ⅲ将瓶中溶液加热到75~80℃,趁热用Ⅰ中配制的高锰酸钾溶液滴定至终点.记录消耗高锰酸钾溶液的体积,计算得出产品纯度.
①滴定过程中反应的离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
②达到滴定终点的标志为锥形瓶中溶液突变为浅红色且半分钟内不褪色.
③加热温度大于90℃,部分草酸发生分解,会导致测得产品纯度偏高.(填“偏高”、“偏低”或“无影响”)
④将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如右图,其原因可能为生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快.
1.由CH4和O2组成的混合气体,标准状况下的密度为1g•L-1,则该混合气体中CH4和O2的质量的量之比为( )
| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:4 |
11.四种基本反应类型判断不正确的是( )
| A. | C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2 化合反应 | |
| B. | CaCO3$\frac{\underline{\;点燃\;}}{\;}$ CaO+CO2↑分解反应 | |
| C. | AgNO3+KCl═AgCl↓+KNO3复分解反应 | |
| D. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 |
18.已知反应:2NO(g)+Br2(g)?2NOBr(g)的活化能为akJ•mol-1,其反应机理如下:
①NO(g)+Br2(g)?NOBr2(g)慢
②NO(g)+NOBr2(g)?2NOBr(g)快
下列有关该反应的说法正确的是( )
①NO(g)+Br2(g)?NOBr2(g)慢
②NO(g)+NOBr2(g)?2NOBr(g)快
下列有关该反应的说法正确的是( )
| A. | 反应速率主要取决于反应②的快慢 | B. | 反应速率v(NO)=v(NOBr)=2v(Br2) | ||
| C. | NOBr2是该反应的催化剂 | D. | 该反应的焓变等于akJ•mol-1 |
15.下列说法不正确的是( )
| A. | 6.02×1023是阿伏加德罗常数的近似值 | |
| B. | 阿伏加德常数个微粒的物质的量是1 mol | |
| C. | 1 mol 12C原子的质量为12 g | |
| D. | 硫酸的摩尔质量是98 g |
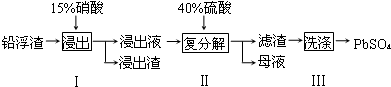
9.废弃物的综合利用既有利于节约资源,又有利于保护环境.工业上利用铅浮渣(主要成分是PbO、Pb还含有少量的Ag、CaO)可制备硫酸铅.制备流程图如图:
下表是25℃时某些盐的浓度积常数:
(1)实验室用75%的硝酸来配制15%的硝酸溶液,不需用到的玻璃仪器有CD(填标号).
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒
(2)步骤I有NO产生,浸出液中含量最多的金属阳离子为 Pb2+,写出Pb参加反应的化学方程式3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O,为防止Ag被溶解进入溶液,步骤I操作时应注意控制硝酸的用量并使Pb稍有剩余.
(3)母液可循环利用于步骤I,其溶质主要是HNO3(填一种物质化学式),若母液中残留的 SO42-过多,循环利用时可能出现的问题是浸出时部分Pb2+生成PbSO4随浸出渣排出,降低PbSO4的产率.
(4)粗PbSO4 产品含有的杂质是CaSO4,需用Pb(NO3)2溶液多次洗涤,以得到纯净的PbSO4.
(5)铅蓄电池放电时正极的电极反应式为PbO2+2e-+4H++SO42-=PbSO4+2H2O.如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.80L,电解前硫酸溶液浓度为4.50mol•L-1,当制得4.48LCl2时(在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)4 mol•L-1.

下表是25℃时某些盐的浓度积常数:
| 化学式 | CaSO4 | Ag2SO4 | PbSO4 |
| Ksp | 4.9×10-5 | 1.2×10-5 | 1.6×10-8 |
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒
(2)步骤I有NO产生,浸出液中含量最多的金属阳离子为 Pb2+,写出Pb参加反应的化学方程式3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O,为防止Ag被溶解进入溶液,步骤I操作时应注意控制硝酸的用量并使Pb稍有剩余.
(3)母液可循环利用于步骤I,其溶质主要是HNO3(填一种物质化学式),若母液中残留的 SO42-过多,循环利用时可能出现的问题是浸出时部分Pb2+生成PbSO4随浸出渣排出,降低PbSO4的产率.
(4)粗PbSO4 产品含有的杂质是CaSO4,需用Pb(NO3)2溶液多次洗涤,以得到纯净的PbSO4.
(5)铅蓄电池放电时正极的电极反应式为PbO2+2e-+4H++SO42-=PbSO4+2H2O.如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.80L,电解前硫酸溶液浓度为4.50mol•L-1,当制得4.48LCl2时(在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)4 mol•L-1.
 .
.