题目内容
11.下列各组物质反应后溶液或固体颜色不发生变化的是( )| A. | 将锌粉投入CuCl2溶液 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 硝酸亚铁溶液中加入稀H2SO4 | D. | 一氧化碳通过灼热的Fe3O4粉末 |
分析 A.Zn的活泼性比Cu强,可发生单质之间的置换反应;
B.二氧化碳与过氧化钠反应生成碳酸钠;
C.硝酸亚铁溶液中加入稀H2SO4时,发生氧化还原反应生成铁离子;
D.CO与四氧化三铁发生氧化还原反应生成Fe.
解答 解:A.将锌粉投入CuCl2溶液,反应生成Cu和氯化锌,溶液为蓝色变为无色,故A不选;
B.二氧化碳与过氧化钠反应生成碳酸钠,观察到固体由淡黄色变为白色,故B不选;
C.硝酸亚铁溶液中加入稀H2SO4时,发生氧化还原反应生成铁离子,则溶液由浅绿色变为黄色,故C不选;
D.CO与四氧化三铁发生氧化还原反应生成Fe,还原性铁粉为黑色,则反应前后均为黑色,故D选;
故选D.
点评 本题考查金属及化合物的性质,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
1.将一小块钠投入下列溶液时,既能产生气体又会出现沉淀的是( )
| A. | 稀H2SO4 | B. | 氢氧化钠溶液 | C. | 氯化铁溶液 | D. | 氯化钾溶液 |
19.下列实验装置设计正确、且能达到目的是( )
| A. | 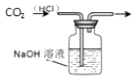 用于除去CO2中的HCl | B. | 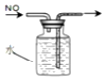 排水法收集NO | ||
| C. | 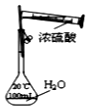 配制一定物质的量浓度的稀硫酸 | D. | 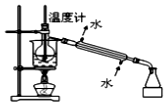 海水的淡化 |
6.在指定的条件下,下列各组离子一定能大量共存的是( )
| A. | 无色的溶液中:Fe3+、K+、NO3-、Cl- | |
| B. | 含有大量Ba2+的溶液中:NH4+、Na+、Cl-、H+ | |
| C. | pH=13的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | c(H+)=0.1 mol•L-1的溶液中:K+、I-、Cl-、NO3- |
12.下列除杂试剂的选择和除杂后检验杂质是否除尽的方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂试剂 | 检验方法 |
| A | CO2(SO2) | 饱和NaHSO3溶液 | 将已除杂质的少量气体通入品红溶液 |
| B | NaHCO3溶液(Na2CO3) | 过量CO2 | 取少量溶液,加入Ca (OH)2溶液,观察现象 |
| C | NO(NO2) | 水 | 观察颜色 |
| D | 乙烷(乙烯) | 酸性KMnO4溶液 | 将已除杂质的少量气体通入溴水 |
| A. | A | B. | B | C. | C | D. | D |
9.某原子的摩尔质量是Mg•mol-1,则一个该原子的真实质量是( )
| A. | $\frac{M}{6.02×1{0}^{23}}$g | B. | $\frac{1}{M}$ g | C. | M g | D. | $\frac{6.02×1{0}^{23}}{M}$ g |
10.下列说法正确的是( )
| A. | 强电解质溶液的导电能力一定比弱电解质溶液的强 | |
| B. | 氧化钠是强电解质,醋酸是弱电解质 | |
| C. | 氨气是弱电解质,铜是强电解质 | |
| D. | 硫酸钠是强电解质,硫酸钡是弱电解质 |