题目内容
在烧杯中加水和苯(密度:0.88g?cm-3)各50ml,将以块金属钠(密度:0.97g?cm-3)投入杯中.观察到的现象可能是( )
| A、钠在水层中反应并四处游动 |
| B、钠停在苯层中不反应 |
| C、钠在苯的液面上反应并四处游动 |
| D、钠在苯与水的界面处反应并可能上下跳动 |
考点:钠的化学性质
专题:几种重要的金属及其化合物
分析:考虑钠与水的反应,结合钠的密度、水和苯的密度大小来分析.
解答:
解:因苯的密度比水小,所以苯在上层,水在下层,又因钠的密度比水小,比苯大,因此介于两者之间,而钠能与水反应产生气体,在与水反应生成气体后被气体带离水层,进入苯层后停止反应又下沉,如此往复,直至钠反应完.
故选D.
故选D.
点评:本题考查钠的性质,难度不大,借助于题目情境,培养了学生分析问题的能力.

练习册系列答案
相关题目
将Cu放入0.1mol?L-1的FeCl3溶液中,反应一定时间后取出Cu,溶液中Fe2+、Fe3+的浓度比为3:2,则Cu2+和Fe3+的物质的量之比为( )
| A、3:2 | B、3:5 |
| C、4:3 | D、3:4 |
“分类”是一种思想方法,在化学发展中起到了重要作用.下列说法正确的是( )
| A、氧化还原反应中,一种元素化合价升高,一定有另一种元素化合价降低 |
| B、根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 |
| C、根据水溶液能否导电将化合物分为电解质和非电解质 |
| D、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示,下列说法正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示,下列说法正确的是( )| A、在相同温度下,同浓度的三种酸溶液的导电能力顺序:HX<HY<HZ | ||
| B、将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中的离子浓度顺序:c(X-)>c(Y-)>c(OH-)>c(H+) | ||
| C、根据滴定曲线,可得Ka(HY)≈10-5 | ||
D、HY与HZ混合,达到平衡时:c(H+)=
|
常温下,下列各组粒子在指定溶液中一定能大量共存的是( )
| A、使甲基橙变红的溶液中:Ag(NH3)2+、H+、Na+、NO3- |
| B、0.1 mol?L-1 Fe3+溶液中:Cl-、SO42-、K+、C6H5OH |
| C、“84”消毒液的水溶液中:K+、Cl-、Na+、OH- |
| D、通入过量SO2气体的溶液中:K+、NO3-、Ba2+、Cl- |
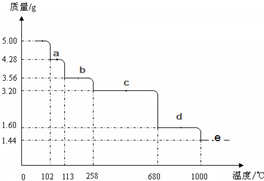
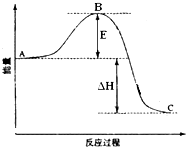 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题: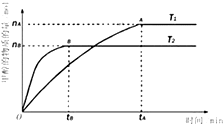 Ⅰ.甲醇是一种新型的能源.
Ⅰ.甲醇是一种新型的能源.