题目内容
某同学通过系列实验探究铝及其化合物的性质,操作正确且能达到目的是( )
| A、将浓氨水缓慢滴入Al2(SO4)3溶液时候,观察Al(OH)3沉淀的生成和溶解 |
| B、将Al(OH)3浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| C、将Al(OH)3沉淀转入蒸发皿中,加热至无水蒸气逸出,得氧化铝固体 |
| D、分别向Al(OH)3沉淀中加入稀硫酸和NaOH溶液,探究Al(OH)3的两性 |
考点:化学实验方案的评价,镁、铝的重要化合物
专题:
分析:A.Al(OH)3能溶于强碱但不溶于弱碱;
B.过滤时需要玻璃棒引流;
C.应灼烧Al(OH)3固体得到氧化铝固体;
D.两性氢氧化物能溶于强碱、强酸溶液.
B.过滤时需要玻璃棒引流;
C.应灼烧Al(OH)3固体得到氧化铝固体;
D.两性氢氧化物能溶于强碱、强酸溶液.
解答:
解:A.Al(OH)3能溶于强碱但不溶于弱碱,一水合氨是弱碱,所以氢氧化铝不溶于氨水,故A错误;
B.过滤时需要玻璃棒引流,否则易导致滤纸弄坏,故B错误;
C.灼烧Al(OH)3固体而不是加热氢氧化铝固体来制取氧化铝固体,故C错误;
D.两性氢氧化物能溶于强碱、强酸溶液,所以可以分别向Al(OH)3沉淀中加入稀硫酸和NaOH溶液,探究Al(OH)3的两性,故D正确;
故选D.
B.过滤时需要玻璃棒引流,否则易导致滤纸弄坏,故B错误;
C.灼烧Al(OH)3固体而不是加热氢氧化铝固体来制取氧化铝固体,故C错误;
D.两性氢氧化物能溶于强碱、强酸溶液,所以可以分别向Al(OH)3沉淀中加入稀硫酸和NaOH溶液,探究Al(OH)3的两性,故D正确;
故选D.
点评:本题以氢氧化铝为载体考查两性氢氧化物性质、氧化铝的制取、基本操作等知识点,侧重考查基本性质、基本操作,注意氢氧化铝不溶于弱碱.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某同学组装了如图所示的电化学装置,电极材料Ⅰ-Ⅳ均为石墨,闭合K后,下列叙述正确的是( )
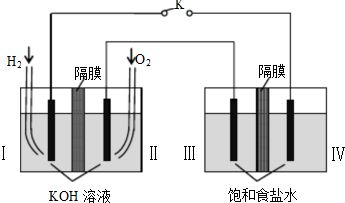

| A、电子流动方向:电极Ⅳ-Ⅰ |
| B、电极Ⅱ电极反应式:O2+2H2O+4e-=4OH- |
| C、电极Ⅲ发生还原反应 |
| D、电极Ⅳ附近观察到黄绿色气体 |
下列叙述正确的是( )
| A、氯气的水溶液可以导电,氯气是电解质 |
| B、在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+ )增大 |
| C、升高温度,可逆反应的化学平衡常数一定增大 |
| D、在 CH3COONa 溶液中加入适量 CH3COOH,可使 c( Na+)=c(CH3COO-) |
已知乙醇、乙酸、正丁醇、乙酸乙酯、乙酸正丁酯的沸点如下:
下列关于实验室制备乙酸乙酯和乙酸正丁酯的描述正确的是( )
| 物质 | 乙酸 | 乙醇 | 正丁醇 | 乙酸乙酯 | 乙酸正丁酯 |
| 沸点(0C) | 117.9 | 78.5 | 117.7 | 77 | 126 |
| A、均采用水浴加热 |
| B、制备乙酸正丁酯时正丁醇过量 |
| C、均采用边反应边蒸馏的方法 |
| D、制备乙酸乙酯时乙醇过量 |
通常用来衡量一个国家的石油化学工业发展水平标志的是( )
| A、石油产量 |
| B、乙烯的产量 |
| C、合成纤维的产量 |
| D、硫酸的产量 |
下列有机物命名正确的是( )
| A、3-甲基-2-戊炔 |
| B、3-乙基-1-丁烯 |
| C、2-甲基-1-丙醇 |
| D、3,4,4-三甲基己烷 |

