题目内容
15. 海水中主要离子的含量如下:
海水中主要离子的含量如下:| 成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
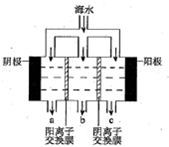
(2)电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.阴极上产生氢气,阴极附近还产生少量白色沉淀,其成分有Mg(OH)2和CaCO3,生成CaCO3的离子方程式是Ca2++OH-+HCO3-=CaCO3↓+H2O.
(3)用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:
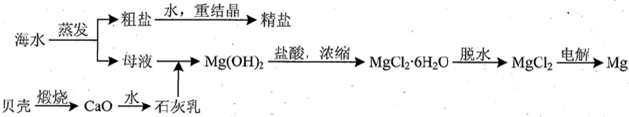
①在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发…洗涤等步骤;有关其中“蒸发”步骤的叙述正确的是bd.
a.蒸发的目的是得到热饱和溶液
b.蒸发的目的是析出晶体
c.应用余热蒸干溶液
d.应蒸发至有较多晶体析出时为止
②由MgCl2溶液得到MgCl2•6H2O晶体时,也需要蒸发,蒸发的目的是得到热饱和溶液,判断溶液已饱和的现象是溶液表面形成晶膜.
(4)25℃时,饱和Mg(OH)2溶液的浓度为5×10-4 mol/L.
①饱和Mg(OH)2溶液中滴加酚酞,现象是溶液变红.
②某学习小组测海水中Mg2+含量(mg/L)的方法是:取一定体积的海水,加入足量盐酸,再加入足量NaOH,将Mg2+转为Mg(OH)2.25℃,该方法测得的Mg2+含量与表中1272mg/L的“真值”比,相对误差约为-5.6%[保留2位小数,海水中饱和Mg(OH)2溶液的密度都以l g/cm3计].
分析 (1)碳酸氢根发生水解呈碱性;
(2)氢离子在阴极上产生氢气,此时阴极中集聚了大量氢氧根离子,并与镁离子生成Mg(OH)2白色沉淀,同时又和碳酸氢根生成碳酸根离子,碳酸根又和钙离子结合生成CaCO3;
(3)①氯化钠的溶解度随温度变化不大,故蒸发的目的不是得到热饱和溶液,而是把水蒸出使晶体析出,最后应蒸发至有较多晶体析出时为止;
②由MgCl2溶液得到MgCl2•6H2O晶体时,也需要蒸发,蒸发的目的是得到热饱和溶液;
(4)①饱和Mg(OH)2溶液呈碱性;
②取一定体积的海水,加入足量盐酸除掉碳酸氢根,再加入足量NaOH,将Mg2+转为Mg(OH)2.由25℃时,饱和Mg(OH)2溶液的浓度为5×10-4 mol/L.求得1L溶液中镁离子的质量为5×10-4mol/L×24g/mol=1200mg/L.25℃,该方法测得的Mg2+含量与表中1272mg/L的“真值”比,相对误差约为$\frac{1200-1272}{1272}×100%$=-5.6%.
解答 解:(1)常温下,海水的pH在7.5~8.6之间,其原因是存在碳酸氢根发生水解呈碱性,离子方程式为HCO3-+H2O?H2CO3+OH-,故答案为:HCO3-+H2O?H2CO3+OH-;
(2)氢离子在阴极上产生氢气,此时阴极中集聚了大量氢氧根离子,并与镁离子生成Mg(OH)2白色沉淀,同时又和碳酸氢根生成碳酸根离子,碳酸根又和钙离子结合生成CaCO3,生成CaCO3的离子方程式是Ca2++OH-+HCO3-=CaCO3↓+H2O,
故答案为:Mg(OH)2;Ca2++OH-+HCO3-=CaCO3↓+H2O;
(3)①氯化钠的溶解度随温度变化不大,故蒸发的目的不是得到热饱和溶液,而是把水蒸出使晶体析出,最后应蒸发至有较多晶体析出时为止,选择bd,
故答案为:bd;
②由MgCl2溶液得到MgCl2•6H2O晶体时,也需要蒸发,蒸发的目的是得到热饱和溶液,判断溶液已饱和的现象是溶液表面形成晶膜,
故答案为:溶液表面形成晶膜;
(4)①饱和Mg(OH)2溶液中滴加酚酞,由于溶液呈碱性,现象是溶液变红,故答案为:溶液变红;
②取一定体积的海水,加入足量盐酸除掉碳酸氢根,再加入足量NaOH,将Mg2+转为Mg(OH)2.由25℃时,饱和Mg(OH)2溶液的浓度为5×10-4 mol/L.求得1L溶液中镁离子的质量为5×10-4mol/L×24g/mol=1200mg/L.25℃,该方法测得的Mg2+含量与表中1272mg/L的“真值”比,相对误差约为$\frac{1200-1272}{1272}×100%$=-5.6%
故答案为:盐酸;-5.6.
点评 本题考查了海水淡化的电渗析原理的分析判断,为高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,海水中溴的提取过程,溶液中得到固体的条件应用,反应过程中的氧化剂计算,注意氯气两次氧化消耗,题目难度中等.

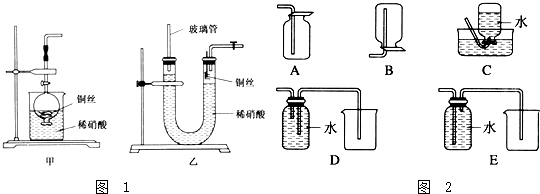
 Na2CO3和NaHCO3与盐酸反应热效应的测定.按如图所示连接好装置,为探究NaHCO3、Na2CO3和盐酸反应过程中的热效应,进行实验并测得如下数据:
Na2CO3和NaHCO3与盐酸反应热效应的测定.按如图所示连接好装置,为探究NaHCO3、Na2CO3和盐酸反应过程中的热效应,进行实验并测得如下数据:| 序号 | 48mL试剂 | 固体 | 混合前温度/℃ | 混合后温度/℃ |
| ① | 水 | 2 g NaHCO3 | 20.0 | 18.6 |
| ② | 水 | 2 g Na2CO3 | 20.0 | 21.6 |
| ③ | 盐酸(0.1mol•L-1) | 2 g NaHCO3 | 20.0 | 17.2 |
| ④ | 盐酸(0.1mol•L-1) | 2 g Na2CO3 | 20.0 | 22.6 |
A.NaHCO3(s)的溶解是放热过程
B.Na2CO3(s)的溶解是吸热过程
C.Na2CO3(s)与盐酸的反应是放热反应
D.仅根据实验③就可以确定HCO3-(aq)+H+(aq)═CO2(g)+H2O(l)△H>0.
| A. | Cl2>Fe3+>Cu2+>MnO2 | B. | MnO2>Cl2>Fe3+>Cu2+ | ||
| C. | Fe3+>Cu2+>MnO2>Cl2 | D. | Cu2+>Fe3+>Cl2>MnO2 |
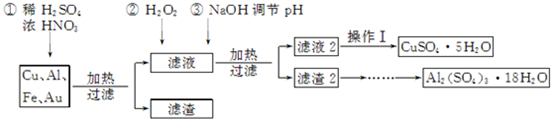
已知:Fe3+、Al3+、Cu2+开始沉淀至沉淀完全的pH范围分别为:2.2~3.2、4.1~5.0、5.3~6.6.
(1)得到滤渣1的主要成分为Au.
(2)操作Ⅰ包含的实验步骤有:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;过滤操作所用到的玻璃仪器有烧杯、玻璃棒和漏斗.
(3)操作Ⅰ中常用无水乙醇对晶体进行洗涤,选用无水乙醇的原因是减少晶体的溶解,便于干燥.
(4)第②步加H2O2后发生反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(5)取上述硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:323K~523K,553K~687K,当温度在1 043K以上不再失重,下表列出了不同温度下的失重率:
[硫酸铝晶体化学式为Al2(SO4)3•18H2O,相对分子质量为666]
已知:失重%=$\frac{加热减少的质量}{原晶体样品的总质量}$×100%.
| 温度(K) | 失重(%) | |
| 第一阶段 | 323~523 | 40.54 |
| 第二阶段 | 553~687 | 48.65 |
| 第三阶段 | 1 043以上 | 84.68 |
①失重第一阶段分解产物的化学式;
②失重第二阶段反应的反应化学方程式.
 .
. .
.