题目内容
8.某烃R与溴水加成产物是2,2,3,3-四溴丁烷,下列物质中与R是同系物的是( )| A. | 乙炔 | B. | 2-丁炔 | C. | 2-丁烯 | D. | 1,3-丁二烯 |
分析 2,2,3,3-四溴丁烷为CH3C(Br)2C(Br)2CH3,由R与溴加成得到,故R为CH3C≡CCH3,R的同系物中应含有1个C≡C三键,符合通式CnH2n-2,与R相差1个或若干个CH2原子团,加成结合选项判断.
解答 解:2,2,3,3-四溴丁烷为CH3C(Br)2C(Br)2CH3,由R与溴加成得到,故R为CH3C≡CCH3,R的同系物中应含有1个C≡C三键,符合通式CnH2n-2,与R相差1个或若干个CH2原子团,R为2-丁炔,
A.乙炔含有1个C≡C三键,符合通式CnH2n-2,与W相差2个CH2原子团,互为同系物,故A正确;
B.R为2-丁炔,是同种物质,故B错误;
C.2-丁烯含有1个C=C双键,不含C≡C三键,二者不是同系物,故C错误;
D.1,3-丁二烯含有2个C=C双键,不含C≡C三键,二者分子式相同,互为同分异构体,故D错误.
故选A.
点评 本题考查加成反应、同系物、同分异构体等,难度不大,注意把握概念的内涵与外延.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
18.下列单质或化合物性质的描述正确的是( )
| A. | NaHSO4水溶液显中性 | |
| B. | NO2溶于水时发生氧化还原反应 | |
| C. | SiO2与酸、碱均不反应 | |
| D. | Fe在足量Cl2中燃烧生成FeCl2和FeCl3 |
19.用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,22.4LO2中一定含有NA个氧原子 | |
| B. | 将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L | |
| C. | 标准状况下,NA个H2O分子的体积是22.4L | |
| D. | 3.4gNH3含有的分子数为0.2NA |
16.下列说法正确的是( )
| A. | 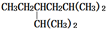 的系统命名法为2,5-二甲基-4-乙基己烷 的系统命名法为2,5-二甲基-4-乙基己烷 | |
| B. | 石油的裂化、煤的气化与液化都属于化学变化,而石油的分馏与煤的干馏都属于物理变化 | |
| C. | 总质量一定时,乙酸和葡萄糖无论以何种比例混合,完全燃烧消耗氧气的量相等 | |
| D. | 油脂、淀粉、蛋白质等高分子化合物都属于混合物,一定条件下均可发生水解 |
3.汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.德国大众汽车尾气检测造假事件引起全世界震惊.根据下列示意图(如图1)回答有关问题:
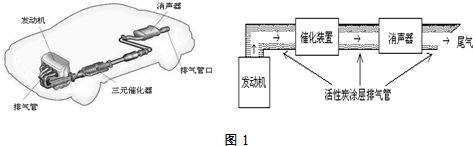
(1)汽车发动机工作时会引发N2(g)+O2(g)=2NO(g)△H=+180kJ•mol-1,其能量变化示意图如下:
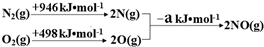
则NO中氮氧键的键能为632kJ•mol-1.
(2)空燃比过小易产生CO.有人提出可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染.判断该设想是否可行,并说出理由不合理,该反应焓增、熵减,任何条件下都不能自发进行或该反应△H>0,△S<0则△G>0.
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口
C.升高排气管温度 D.添加合适的催化剂
(4)催化装置中涉及的反应之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).
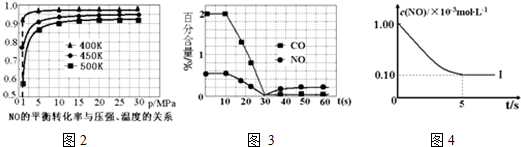
①探究上述反应中NO的平衡转化率与压强、温度的关系,得到图2所示的曲线.催化装置比较适合的温度和压强是400K,1MPa.
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图3所示.则前10s 内,CO和NO百分含量没明显变化的原因是尚未达到催化剂工作温度(或尚未达到反应的温度).
③研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
根据坐标图4,计算400K时该反应的平衡常数为5000L•mol-1;并在图中画出上表中的实验Ⅱ、Ⅲ条件下混合气体中NO浓度随时间变化的趋势曲线图(标明各条曲线的实验编号).

(1)汽车发动机工作时会引发N2(g)+O2(g)=2NO(g)△H=+180kJ•mol-1,其能量变化示意图如下:

则NO中氮氧键的键能为632kJ•mol-1.
(2)空燃比过小易产生CO.有人提出可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染.判断该设想是否可行,并说出理由不合理,该反应焓增、熵减,任何条件下都不能自发进行或该反应△H>0,△S<0则△G>0.
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口
C.升高排气管温度 D.添加合适的催化剂
(4)催化装置中涉及的反应之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).

①探究上述反应中NO的平衡转化率与压强、温度的关系,得到图2所示的曲线.催化装置比较适合的温度和压强是400K,1MPa.
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图3所示.则前10s 内,CO和NO百分含量没明显变化的原因是尚未达到催化剂工作温度(或尚未达到反应的温度).
③研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
| 实验编号 | T(K) | NO初始浓度 (mol•L-1) | CO初始浓度 (mol•L-1) | 催化剂的比表面积(m2/g) |
| Ⅰ | 400 | 1.00×10-3 | 3.60×10-3 | 82 |
| Ⅱ | 400 | 1.00×10-3 | 3.60×10-3 | 124 |
| Ⅲ | 450 | 1.00×10-3 | 3.60×10-3 | 124 |
13.下列关于测定1mol氢气体积的操作中,错误的是( )
| A. | 保证装置不漏气 | |
| B. | 镁带称量后,用砂皮擦去表面的氧化层 | |
| C. | 用针筒注入硫酸后,拔出速度要快 | |
| D. | 镁带的质量要使产生的氢气足以计量 |
20.m mol C2H2跟n mol H2发生加成反应,当其达到平衡时,生成p mol C2H4.将平衡的混合气体完全燃烧后生成二氧化碳和水,所需氧气的物质的量是多少摩尔( )
| A. | 3m+n | B. | $\frac{5}{2}$m+$\frac{1}{2}$n-p | C. | $\frac{5}{2}$m+$\frac{1}{2}$n | D. | 3m+n+2p |
17.将过量的二氧化碳分别通入下列溶液,最终溶液中有沉淀析出的是( )
| A. | 氯化钙溶液 | B. | 硅酸钠溶液 | C. | 澄清石灰水 | D. | 饱和碳酸钠溶液 |
4.下列电离方程式中正确的是( )
| A. | NaHCO3溶于水:NaHCO3═Na++H++CO32- | |
| B. | H2CO3?2H++CO32- | |
| C. | Al(OH)3酸式电离:Al(OH)3═H2O+AlO2-+H+ | |
| D. | NaHSO4熔化:NaHSO4═Na++HSO4- |