题目内容
溴是海水中重要的非金属元素,地球上90%的溴元素以Br-的形式存在于海水中,所以人们称溴为“海洋元素”,下列有关说法中正确的是(( )
| A、从海水中提取溴时,不涉及氧化还原反应 |
| B、苯与溴水反应生成溴苯 |
| C、可以用CCl4萃取溴水中的溴 |
| D、向FeBr2溶液中通入Cl2时,一定会发生如下反应:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
考点:氧化还原反应,氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:A、海水中溴以离子形式存在,需要氧化还原反应生成溴单质;
B、苯与溴水不反应;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶;
D、Fe2+的还原性强于溴离子点的还原性,若氯气少量,只氧化Fe2+.
B、苯与溴水不反应;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶;
D、Fe2+的还原性强于溴离子点的还原性,若氯气少量,只氧化Fe2+.
解答:
解:A、海水中溴以离子形式存在,需要氧化还原反应生成溴单质,故A错误;
B、苯与溴水不反应,苯与液溴在催化剂的条件下反应生成溴苯,故B错误;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶,可以用CCl4萃取溴水中的溴,故C正确;
D、Fe2+的还原性强于溴离子的还原性,若氯气少量,只氧化Fe2+,若氯气过量,一定会全部氧化Fe2+和溴离子,故D错误.
故选:C.
B、苯与溴水不反应,苯与液溴在催化剂的条件下反应生成溴苯,故B错误;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶,可以用CCl4萃取溴水中的溴,故C正确;
D、Fe2+的还原性强于溴离子的还原性,若氯气少量,只氧化Fe2+,若氯气过量,一定会全部氧化Fe2+和溴离子,故D错误.
故选:C.
点评:本题考查了非金属元素的性质及单质的性质、氧化还原反应的判断,注意氧化性Cl2>Br2>Fe3+,题目难度不大.

练习册系列答案
相关题目
碳原子数小于或等于8的单烯烃,与HBr加成反应的产物只有一种结构,符合条件的单烯烃(不考虑反异构和立体异构)( )
| A、4种 | B、5种 | C、6种 | D、7种 |
下列变化中,属于放热反应的是( )
| A、H2O(g)═H2O(l)△H=-44kJ/mol |
| B、2HI(g)═H2(g)+I2(g)△H=+14.9kJ/mol |
C、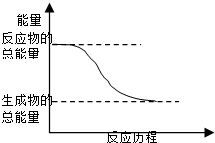 能量变化如图所示的化学反应 |
| D、形成化学键时放出能量的化学反应 |
用NA代表阿伏加德罗常数,相关说法不正确的是( )
| A、13.5 g Al与足量盐酸反应生成H2的分子数为NA |
| B、标准状况下,2.24 L CH4所含电子数为NA |
| C、500 mL 1 mol?L-1的K2SO4溶液中含有K+数目为NA |
| D、0.5 mol O2和0.5 mol O3的混合物所含有的氧原子个数为2.5NA |
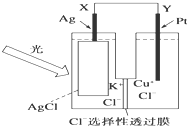 一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)
一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)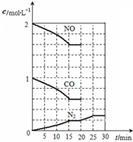 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.