题目内容
20.标准状况下,560mL某气体A的质量为0.75g,则其摩尔质量为30g/mol;已知该气体在水中的溶解度为448(气体溶解度指该气体在压强为101kPa,0℃时,溶解在1体积水里达到饱和状态时的气体的体积),则得到的饱和溶液中溶质A的质量分数为37.5%(A不与水反应),若测得该溶液密度为1.24g/cm3,则该溶液的物质的量浓度为15.5mol/L.分析 根据n=$\frac{V}{{V}_{m}}$、M=$\frac{m}{n}$计算出该气体的摩尔质量;设水的体积为1L,则该气体体积为448L,根据m=nM=$\frac{V}{{V}_{m}}$M计算出该气体的质量,从而可知该溶液质量,再根据ω=$\frac{{m}_{溶质}}{{m}_{溶液}}$×100%计算出所得溶液的质量分数;根据c=$\frac{1000ρω}{M}$计算出该溶液的物质的量浓度.
解答 解:标准状况下,560mL某气体A的质量为0.75g,该气体的物质的量为:$\frac{0.56L}{22.4L/mol}$=0.025mol,其摩尔质量为:M=$\frac{0.75g}{0.025mol}$=30g/mol;
该气体在水中的溶解度为448,设水的体积为1L,则1L水中最多溶解该气体的体积为448L,标准状况下448L气体的物质的量为:$\frac{448L}{22.4L/mol}$=20mol,其质量为:30g/mol×20mol=600g,1L水的质量约为1000g,则得到的饱和溶液中溶质A的质量分数为:$\frac{600g}{1000g+600g}$×100%=37.5%;
若测得该溶液密度为1.24g/cm3,则该溶液的物质的量浓度为:c=$\frac{1000ρω}{M}$=$\frac{1000×1.24×37.5%}{30}$mol/L=15.5mol/L,
故答案为:30g/mol;37.5%;15.5mol/L.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确物质的量浓度与溶质质量分数的关系为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
10.常温时,pH=14和pH=10的两种NaOH溶液等体积混合,所得溶液中c(H+)是( )
| A. | pH>7 | B. | pH=7 | C. | pH<7 | D. | 无法确定 |
11.下列说法中正确的是( )
| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 | |
| B. | 1 L一氧化碳气体一定比1 L氧气的质量小 | |
| C. | 28 g N2和CO的混合气体在标准状况下的体积约为22.4 L | |
| D. | 常温常压下,1 mol碳完全燃烧消耗22.4 L氧气 |
8.唐山市曹妃甸区10月20日的空气质量日报如表:
下列情况对表中三个空气质量指标不会产生影响的是( )
| 项目 | 空气污染指数 | 空气质量级别 | 空气质量 |
| 可吸入颗粒物 | 65 | Ⅱ | 良 |
| 二氧化硫 | 6 | ||
| 二氧化氮 | 20 |
| A. | 用氢气作燃料 | B. | 露天焚烧垃圾 | ||
| C. | 大量排放汽车尾气 | D. | 用煤作燃料 |
15.某化学小组通过查阅资料,设计了如图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
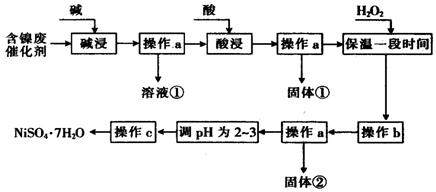
部分阳离子以氢氧化物形式沉淀时的pH如表:
(1)“碱浸”过程中发生反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2OH-═2AlO2-+3H2O
(2)“酸浸”时所加入的酸是H2SO4 (填化学式).
(3)加入H2O2时发生反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2≤PH<7.1.

部分阳离子以氢氧化物形式沉淀时的pH如表:
| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ai(OH)2 | 7.1 | 9.2 |
(2)“酸浸”时所加入的酸是H2SO4 (填化学式).
(3)加入H2O2时发生反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2≤PH<7.1.
5.在无色、碱性溶液中能大量共存的一组离子是( )
| A. | Ca2+、Na+、SO42-、CO32- | B. | K+、Fe2+、SO42-、MnO4- | ||
| C. | Ba2+、K+、Al3+、Cl- | D. | Na+、Ba2+、Cl-、NO3- |
12.既能用浓硫酸干燥又能用碱石灰干燥的气体是( )
| A. | Cl2 | B. | CO2 | C. | O2 | D. | NH3 |