题目内容
下列变化过程中,△S<0的是( )
| A、氯化铵晶体溶于水中 |
| B、NO(g)和O2(g)反应生成NO2(g) |
| C、碘晶体受热升华 |
| D、BaCO3(s)分解为BaO(s)和CO2(g) |
考点:焓变和熵变
专题:
分析:熵变是反应体系的混乱度,是体系混乱度(或无序度)的量度,同一物质,气态熵大于液态熵,液态熵大于固态熵;不同物质生成的气体体积越大,熵值增加,熵变为正值.气体体积减少,熵值减小,熵变为负值,以此解答该题.
解答:
解:A.氯化铵晶体溶于水中变化过程中固体溶解到水中形成溶液,熵值增大,△S>0,故A错误;
B.NO(g)和O2(g)反应生成NO2(g),发生2NO+O2=2NO2,气体的总量减少,熵值减小,△S<0,故B正确;
C.升华变化过程中固体变化为气体,熵值增大,△S>0,故C错误;
D.BaCO3(s)分解为BaO(s)和CO2(g),熵值增大,△S>0,故D错误;
故选:B.
B.NO(g)和O2(g)反应生成NO2(g),发生2NO+O2=2NO2,气体的总量减少,熵值减小,△S<0,故B正确;
C.升华变化过程中固体变化为气体,熵值增大,△S>0,故C错误;
D.BaCO3(s)分解为BaO(s)和CO2(g),熵值增大,△S>0,故D错误;
故选:B.
点评:本题考查了熵变的判断,为高频考点,侧重于学生的分析能力的考查,题目难度不大,明确反应过程或变化过程中微粒的变化、气体体积的变化是解题关键.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
现有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Ba2+、CO32-、Cl-、SO42--.现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.根据上述实验,以下推测正确的是( )
| A、一定存在K+、NH4+、CO32-、SO42-,一定不存在Ba2+、Cl- |
| B、一定存在NH4+、Cl-、CO32-、SO42-,可能存在K+ |
| C、c(SO42-)=0.2mol?L-1,c(NH4+)>c(SO42-) |
| D、如果溶液中存在NH4+、Cl-、CO32-、SO42-、K+五种离子,则c(K+)>0.2mol?L-1 |
已知常温时ksp(AgCl)=1.8×10-10、ksp(AgBr)=4.9×10-13,将AgCl和AgBr的饱和溶液等体积混合,再加足量浓AgNO3溶液,发生的反应为( )
| A、只有AgBr沉淀生成 |
| B、AgCl和AgBr沉淀等量生成 |
| C、AgCl沉淀少于AgBr沉淀 |
| D、AgCl沉淀多于AgBr沉淀 |
在通常条件下,下列各组物质的性质排列顺序正确的是( )
| A、熔点:SiO2>SiCl4>KCl |
| B、水溶性:HCl>CO2>SO2 |
| C、沸点:乙烷>戊烷>丁烷 |
| D、热稳定性:HF>H2O>NH3 |
化学转移反应是一种固体或液体物体A在一定温度下与一种气体物体B反应,先形成气相产物,该气相产物在体系的不同温度部分又发生逆反应,结果重新得到A的反应,下图为固体物质A发生转移反应的理想装置,在原料放置区(即图中T1段),A和B尽可能生成C并向沉淀区移动,在沉淀区(T2)段,C尽可能分解沉积出A.下列说法不正确的是( )
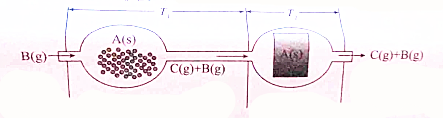

| A、温度和浓度是反应的重要要素 |
| B、绝大多数化学转移反应应在真空中进行 |
| C、对于化学转移反应A(s)+B(g)?C(g),降低C的浓度,平衡正向移动 |
| D、用化学转移反应制备TaS2,晶体:2TaI5(s)+2S2(g)?5I2(g)+2TaS2(s)△H>0,T1应该小于T2 |


