题目内容
常温下,等体积、等物质的浓度的NaCl和CH3COONa溶液中的阴离子总数相比( )
| A、前者多 | B、后者多 |
| C、一样多 | D、无法判断 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:根据物质在溶液中电离出来的离子多少以及离子水解程度分析解答,CH3COONa为强碱弱酸盐,水解显碱性,据此解答该题.
解答:
解:CH3COONa溶于水,能发生水解反应,消耗1个CH3COO-,生成1个OH-和1个CH3COOH,所以阴离子数目不变,氯化钠电离生成阴离子Cl-;在考虑NaCl和CH3COONa时,因为本身电离或水解产生的阴离子数相等,但是要考虑水的电离,CH3COONa溶液中的阴离子总数略大.
故选B.
故选B.
点评:本题考查了溶液中离子浓度大小比较,同时考查了盐的水解,弱电解质的电离等,题目难度中等.

练习册系列答案
相关题目
下列不饱和化合物(单体)能在一定条件下发生加聚反应生成如图所示物质的是:( )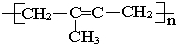
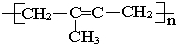
| A、丙烯 |
| B、2-甲基-1,3-丁二烯 |
| C、乙烯和丙烯 |
| D、2-甲基-2-丁烯 |
苹果汁是人们喜爱的饮料.由于饮料中含有 Fe2+离子,现榨的苹果汁在空气中会由淡绿色变为棕黄色,使Fe2+转变为Fe3+离子.若榨苹果汁时加入维生素C,可有效防止这种现象的发生.这说明维生素C具有( )
| A、氧化性 | B、还原性 |
| C、酸性 | D、碱性 |
下列反应活化能最小的是( )
| A、2H2+O2=2H2O |
| B、3H2+O3=3H2O |
| C、2H+O=H2O |
| D、H2+Cl2=2HCl |
在标准状况下,进行甲、乙、丙三组实验:三组各取60mL同浓度盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
则下列说法正确的是( )
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A、甲组和乙组的实验中,盐酸均是过量的 |
| B、盐酸的物质的量浓度为0.8mol/L |
| C、合金中镁铝的物质的量之比为1:1 |
| D、丙组中铝的物质的量为0.018mol |
分子式为C10H14的烃,有一个苯环、两个取代基,其可能的结构有( )
| A、3种 | B、6种 | C、7种 | D、9种 |
将2mol A和1mol B充入某密闭容器中发生反应:2A(g)+B(g)?xC(g),达到化学平衡后,C的体积分数为a.假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是(双选)( )
| A、若在恒温恒压下,当x=1时,按1.5 mol A、1 mol C作为起始物质,达到平衡后,C的体积分数仍为a |
| B、若在恒温恒容下,当x=2时,将2molC作起始物质,达到平衡后,C的体积分数仍为a |
| C、若在恒温恒压下,当x=3时,1mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为a |
| D、若在恒温恒容下,按0.6mol A、0.3mol B、1.4mol C作起始物质,达到平衡后,C的体积分数仍为a,则x一定为2或3 |
有关甲烷和丙烷的说法中,错误的是( )
| A、互为同系物 |
| B、均不能使高锰酸钾酸性溶液褪色 |
| C、等质量燃烧消耗氧气甲烷多 |
| D、甲烷没有同分异构体而丙烷有两种同分异构体 |