题目内容
一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A、N2、H2和NH3的物质的量分数不再改变 |
| B、c(N2):c(H2):c(NH3)=1:3:2 |
| C、单位时间每增加1molN2,同时增加2mol NH3 |
| D、N2与H2的物质的量之和是NH3的2倍 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:当可逆反应中正逆反应速率相等时,该反应达到平衡状态,反应体系中各物质的物质的量不变、物质的量浓度不变、百分含量不变以及引起的其它一系列物理量不变,据此分析解答.
解答:
解:A.N2、H2和NH3的物质的量分数不再改变时正逆反应速率相等,所以该反应达到平衡状态,故A正确;
B.c(N2):c(H2):c(NH3)=1:3:2时该反应不一定达到平衡状态,与反应物初始量及转化率有关,故B错误;
C.单位时间每增加1molN2,同时增加2mol NH3,即同时也减少2mol NH3,正逆反应速率相等,则该反应达到平衡状态,故C正确;
D.N2与H2的物质的量之和是NH3的2倍时,该反应不一定达到平衡状态,与反应物初始量、转化率有关,故D错误;
故选AC.
B.c(N2):c(H2):c(NH3)=1:3:2时该反应不一定达到平衡状态,与反应物初始量及转化率有关,故B错误;
C.单位时间每增加1molN2,同时增加2mol NH3,即同时也减少2mol NH3,正逆反应速率相等,则该反应达到平衡状态,故C正确;
D.N2与H2的物质的量之和是NH3的2倍时,该反应不一定达到平衡状态,与反应物初始量、转化率有关,故D错误;
故选AC.
点评:本题考查化学平衡状态的判断,只有反应前后改变的物理量才能作为判断依据,为常考查点,易错选项是B,题目难度不大.

练习册系列答案
相关题目
在10L密闭容器中,1mol A和3mol B在一定条件下反应:A(g)+xB(g)?2C(g),2min后达到平衡,生成0.4mol C,测得混合气体共3.4mol,则下列结果正确的是( )
| A、平衡时,物质的量之比n(A):n(B):n(C)=2:11:4 |
| B、x值等于3 |
| C、A的转化率为20% |
| D、B的平均反应速率为0.4 mol/(L?min) |
下列叙述正确的是( )
| A、工业上用电解熔融氯化铝和冰晶石的混合物的方法得到铝 |
| B、一次电池是最常见的化学电源,一次电池中发生氧化还原反应的物质大部分被消耗后就不能再使用,铅蓄电池是最常见的一次电池 |
| C、氯碱工业中,氢氧化钠在电解槽的阴极区产生 |
| D、合成氨生产中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
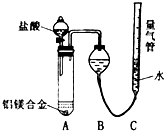 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.请填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.请填写下列空白.