题目内容
太阳能电池是利用光电效应实现能量变化的一种新型装置,目前多采用单晶硅和多晶硅作为基础材料.高纯度的晶体硅可通过以下反应获得:
反应①(合成炉):Si(粗)+3HCl(g)
SiHCl3+H2(g)△H1
反应②(还原炉):SiHCl3+H2(g)
Si(纯)+3HCl(g)△H2
有关物质的沸点如下表所示:
请回答以下问题:
(1)太阳能电池的能量转化方式为 ;由合成炉中得到的SiHCl3往往混有硼、磷、砷、铝等氯化物杂质,分离出SiHCl3的方法是
(2)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应①的KP= ;
(3)对于反应②,在0.1Mpa下,不同温度和氢气配比(
)对SiHCl3剩余量的影响如下表所示:
①该反应的△H2 0(填“>”、“<”、“=”)
②按氢气配比5:1投入还原炉中,反应至4min时测得HCl的浓度为0.12mol?L-1,则SiHCl3在这段时间内的反应速率为 .
③对上表的数据进行分析,在温度、配比对剩余量的影响中,还原炉中的反应温度选择在1100℃,而不选择775℃,其中的一个原因是在相同配比下,温度对SiHCl3剩余量的影响,请分析另一原因是 .
(4)对于反应②,在1100℃下,不同压强和氢气配比(
)对SiHCl3剩余量的影响如图一所示:
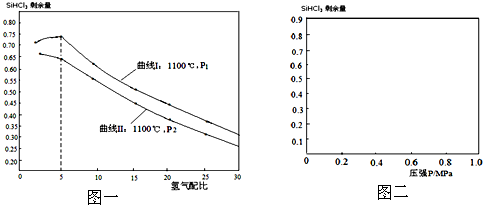
①图中P1 P2(填“>”、“<”、“=”)
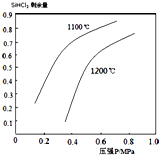
②在图二中画出氢气配比相同情况下,1200℃和1100℃的温度下,系统中SiHCl3剩余量随压强变化的两条变化趋势示意图.
反应①(合成炉):Si(粗)+3HCl(g)
| 280℃-300℃ |
| CuCl |
反应②(还原炉):SiHCl3+H2(g)
| 1100℃ |
有关物质的沸点如下表所示:
| 物质 | BCl3 | PCl3 | SiCl4 | AsCl3 | AlCl3 | SiHCl3 |
| 沸点 | 12.1 | 73.5 | 57.0 | 129.4 | 180(升华) | 31.2 |
(1)太阳能电池的能量转化方式为
(2)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应①的KP=
(3)对于反应②,在0.1Mpa下,不同温度和氢气配比(
| H2 |
| SiHCl3 |
| 配比 剩余量 温度 |
50 | 30 | 25 | 20 | 15 | 10 | 5 | 2 |
| 775℃ | 0.8286 | 0.8476 | 0.8519 | 0.8555 | 0.8579 | 0.8570 | 0.8456 | 0.8422 |
| 1100℃ | 0.2899 | 0.3860 | 0.4169 | 0.4512 | 0.4895 | 0.5312 | 0.5707 | 0.5710 |
②按氢气配比5:1投入还原炉中,反应至4min时测得HCl的浓度为0.12mol?L-1,则SiHCl3在这段时间内的反应速率为
③对上表的数据进行分析,在温度、配比对剩余量的影响中,还原炉中的反应温度选择在1100℃,而不选择775℃,其中的一个原因是在相同配比下,温度对SiHCl3剩余量的影响,请分析另一原因是
(4)对于反应②,在1100℃下,不同压强和氢气配比(
| H2 |
| SiHCl3 |

①图中P1
②在图二中画出氢气配比相同情况下,1200℃和1100℃的温度下,系统中SiHCl3剩余量随压强变化的两条变化趋势示意图.
考点:物质的量或浓度随时间的变化曲线,化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:(1)根据能量的转化方式回答;根据表中数据可知SiHCl3的沸点较低,可采用蒸馏的方式提纯;
(2)利用浓度平衡常数表达式的知识迁移应用到压强平衡常数;
(3)①比较SiHCl3和氢气配比相同时,比较775℃时和1100℃时,SiHCl3剩余的量,判断热效应;
②利用HCl浓度变化量,计算出HCl的反应速率,根据计量数之比等于反应速率之比,得到SiHCl3的反应速率;
③比较相同和氢气相同配比时,比较775℃时和1100℃时,SiHCl3剩余的量,看哪个温度下氢气配比对SiHCl3剩余量影响明显,得到答案;
(4)①比较反应②前后气体体积大小,压强增大使SiHCl3剩余量增大,判断P1和P2大小;
②反应②,正反应方向气体体积增大,压强增大则SiHCl3剩余量增大;正反应方向吸热,温度升高则SiHCl3剩余量增大,据此画出图象.
(2)利用浓度平衡常数表达式的知识迁移应用到压强平衡常数;
(3)①比较SiHCl3和氢气配比相同时,比较775℃时和1100℃时,SiHCl3剩余的量,判断热效应;
②利用HCl浓度变化量,计算出HCl的反应速率,根据计量数之比等于反应速率之比,得到SiHCl3的反应速率;
③比较相同和氢气相同配比时,比较775℃时和1100℃时,SiHCl3剩余的量,看哪个温度下氢气配比对SiHCl3剩余量影响明显,得到答案;
(4)①比较反应②前后气体体积大小,压强增大使SiHCl3剩余量增大,判断P1和P2大小;
②反应②,正反应方向气体体积增大,压强增大则SiHCl3剩余量增大;正反应方向吸热,温度升高则SiHCl3剩余量增大,据此画出图象.
解答:
解:(1)利用太阳的光照获得电流,是利用太阳能转化为电能;根据表中数据可知SiHCl3的沸点较低,可采用分馏的方式提纯,故答案为:太阳能转化为电能、分馏;
(2)利用浓度平衡常数表达式的知识迁移应用到压强平衡常数,则压强平衡常数为生成物气体分压的系数次幂的乘积与反应物气体分压系数次幂乘积的比值,则Kp=
,故答案为:
;
(3)①SiHCl3和氢气配比相同时,775℃时的SiHCl3剩余量大于1100℃时的SiHCl3剩余量,可知温度升高,平衡向逆反应方向移动,正反应方向吸热,即△H2>0,故答案为:>;
②反应至4min时测得HCl的浓度为0.12mol?L-1,则v(HCl)=
=0.03mol.L-1.min-1,计量数之比等于反应速率之比,v(SiHCl3)=
×0.03mol.L-1.min-1=0.01mol.L-1.min-1,故答案为:0.01mol.L-1.min-1;
③相同和氢气相同配比时,在1100℃时,氢气配比对SiHCl3剩余量影响明显,而在775℃时,氢气配比对SiHCl3的剩余量影响不明显,故答案为:在1100℃时,氢气配比对SiHCl3剩余量影响明显,而在775℃时,氢气配比对SiHCl3的剩余量影响不明显;
(4)①比较反应②前后气体体积大小,压强增大使SiHCl3剩余量增大,观察图象可知P1的曲线在上侧,即P1压强下SiHCl3剩余量大,P1>P2,故答案为:>;
②反应②,正反应方向气体体积增大,压强增大则SiHCl3剩余量增大;正反应方向吸热,温度升高则SiHCl3剩余量增大,据此画出图象:
 ,故答案为:
,故答案为: .
.
(2)利用浓度平衡常数表达式的知识迁移应用到压强平衡常数,则压强平衡常数为生成物气体分压的系数次幂的乘积与反应物气体分压系数次幂乘积的比值,则Kp=
| PH2?PSiHCl3 | ||
|
| PH2?PSiHCl3 | ||
|
(3)①SiHCl3和氢气配比相同时,775℃时的SiHCl3剩余量大于1100℃时的SiHCl3剩余量,可知温度升高,平衡向逆反应方向移动,正反应方向吸热,即△H2>0,故答案为:>;
②反应至4min时测得HCl的浓度为0.12mol?L-1,则v(HCl)=
| 0.12mol?L-1 |
| 4min |
| 1 |
| 3 |
③相同和氢气相同配比时,在1100℃时,氢气配比对SiHCl3剩余量影响明显,而在775℃时,氢气配比对SiHCl3的剩余量影响不明显,故答案为:在1100℃时,氢气配比对SiHCl3剩余量影响明显,而在775℃时,氢气配比对SiHCl3的剩余量影响不明显;
(4)①比较反应②前后气体体积大小,压强增大使SiHCl3剩余量增大,观察图象可知P1的曲线在上侧,即P1压强下SiHCl3剩余量大,P1>P2,故答案为:>;
②反应②,正反应方向气体体积增大,压强增大则SiHCl3剩余量增大;正反应方向吸热,温度升高则SiHCl3剩余量增大,据此画出图象:
 ,故答案为:
,故答案为: .
.
点评:本题考查化学反应速率及化学平衡图象,注意把握曲线的变化趋势,正确判断外界条件对平衡移动的影响,明确图象中纵横坐标及点、线、面的意义,难度中等.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 0.1mol?L-1的乙酸溶液中含有的氧原子数0.2NA |
| B、标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA |
| C、标准状况下,23g CH3CH2OH中含有的分子数目为0.5NA |
| D、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |