题目内容
19.有X、Y两种有机物,请按要求回答下列问题:(1)取1.5g有机物X,将其完全燃烧后生成1.8gH2O和1.68LCO2(标准状况),已知该有机物的蒸气对氢气的
相对密度为30,则该有机物的分子式为:C3H8O.
(2)有机物Y的结构可能有
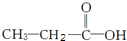 和
和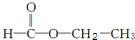 两种,为对其结构进行物理方法鉴定,常用红外光谱和核磁共振氢谱法.
两种,为对其结构进行物理方法鉴定,常用红外光谱和核磁共振氢谱法.①有机物Y若为
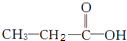 ,则红外光谱中应该有5个吸收峰;核磁共振氢谱中应有4个吸收峰.
,则红外光谱中应该有5个吸收峰;核磁共振氢谱中应有4个吸收峰.②有机物Y若为
 ,则红外光谱中应该有4个吸收峰;核磁共振氢谱中应有3个吸收峰.
,则红外光谱中应该有4个吸收峰;核磁共振氢谱中应有3个吸收峰.
分析 (1)根据相对密度计算X的相对分子质量,再计算X、二氧化碳、水的物质的量,根据原子守恒计算C、H原子数目,结合相对分子质量计算O原子数目;
(2)不同的化学键或官能团吸收频率不同,红外光谱图中处于不同的位置,一般原子之间形成的不同化学键种类等于吸收峰数;核磁共振氢谱吸收峰等于分子中H原子种类.
解答 解:(1)X的相对分子质量为30×2=60,故1.5g X的物质的量为$\frac{1.5g}{60g/mol}$=0.025mol,
二氧化碳物质的量为$\frac{1.68L}{22.4L/mol}$=0.075mol,水的物质的量为$\frac{1.8g}{18g/mol}$=0.1mol,
故X分子中C原子数目为$\frac{0.075mol}{0.025mol}$=3,H原子数目为$\frac{0.1mol×2}{0.025mol}$=8,则O原子数目为$\frac{60-12×3-8}{16}$=1,
故X的分子式为C3H8O,
故答案为:C3H8O;
(2)①有机物Y若为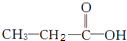 ,含有C-H、C-C、C-O、C=O、O-H键,红外光谱中应该有5个吸收峰;分子中含有3种化学环境不同的H原子,核磁共振氢谱中应有3个吸收峰,
,含有C-H、C-C、C-O、C=O、O-H键,红外光谱中应该有5个吸收峰;分子中含有3种化学环境不同的H原子,核磁共振氢谱中应有3个吸收峰,
故答案为:5;3;
②有机物Y若为 ,含有C-H、C-C、C-O、C=O键,红外光谱中应该有4个吸收峰;分子中含有3种化学环境不同的H原子,核磁共振氢谱中应有3个吸收峰,
,含有C-H、C-C、C-O、C=O键,红外光谱中应该有4个吸收峰;分子中含有3种化学环境不同的H原子,核磁共振氢谱中应有3个吸收峰,
故答案为:4;3.
点评 本题考查有机物分子式与结构的确定,掌握燃烧法利用原子守恒确定有机物分子式,注意对质谱图、红外光谱法、核磁共振氢谱的简单识读.

练习册系列答案
相关题目
9.下列离子反应方程式正确的是( )
| A. | 向Al2(S04)3溶液中加入过量氨水:A3++4NH3•H2O═AlO-+4NH4++2H2O | |
| B. | 少量双氧水滴人酸性KI溶液:2H202+2I-═2H++4H20+I2 | |
| C. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++N03-═3Fe3++NO+2H2O | |
| D. | 碱性锌锰电池正极反应:2MnO2+2H2O+2e一═2MnOOH+2OH- |
10.利用化石燃料开采、加工过程产生的H2S废气,通过电化学法制取氢气的工艺如图,下列说法不正确的是( )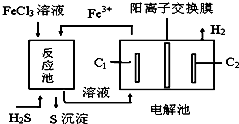

| A. | 电解池中惰性电极C1为阳极 | |
| B. | 该工艺优点之一是FeCl3溶液可循环利用 | |
| C. | 反应池中的离子方程式:2Fe3++S2-=2Fe2++S↓ | |
| D. | 电解池总反应的化学方程式:2FeCl2+2HCl$\frac{\underline{\;通电\;}}{\;}$2FeCl3+H2↑ |
7.下列有关物质(括号内为杂质)的除杂试剂和分离方法均正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 乙醇(乙酸) | KOH溶液 | 分液 |
| C | 苯(苯酚) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
15.U、V、W、Y是原子序数依次增大的短周期主族元素,U、Y在周期表中的相对位置如表;U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.
根据题意完成下列填空:
(1)元素W的原子核外共有5种不同能级的电子.
(2)下列反应在恒容密闭容器中进行:2YO2(g)+O2(g)$?_{催化剂}^{450℃}$ 2YO3(g)+190kJ
①该反应 450℃时的平衡常数大于500℃时的平衡常数(填“大于”、“小于”或“等于”).
②下列描述中能说明上述反应已达平衡的是bd
a.ν(O2)正=2ν(YO3)逆 b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
③在一个固定容积为5L的密闭容器中充入0.20 mol YO2和0.10molO2,半分钟后达到平衡,测得容器中含YO30.18mol,则ν(O2)=0.36mol•L-1•min-1:若继续通入0.20molYO2和0,.10molO2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36mol<n(YO3)<0.40mol.
(3)V的最简单气态氢化物甲的水溶液显碱性.
一定条件下,甲在恒容密闭容器中发生分解反应(正反应放向为吸热反应)并达平衡后,仅改变下表中反应条件x,下列各项中y随x的增大而增大的是bc.(选填序号).
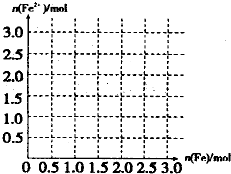
(4)向含4mol V的最高价含氧酸的稀溶液中,逐渐加入Fe粉至过量.假设生成的气体只有一种,请在坐标系中画出n(Fe2+)随n(Fe)变化的示意图.
| U | ||
| Y |
(1)元素W的原子核外共有5种不同能级的电子.
(2)下列反应在恒容密闭容器中进行:2YO2(g)+O2(g)$?_{催化剂}^{450℃}$ 2YO3(g)+190kJ
①该反应 450℃时的平衡常数大于500℃时的平衡常数(填“大于”、“小于”或“等于”).
②下列描述中能说明上述反应已达平衡的是bd
a.ν(O2)正=2ν(YO3)逆 b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
③在一个固定容积为5L的密闭容器中充入0.20 mol YO2和0.10molO2,半分钟后达到平衡,测得容器中含YO30.18mol,则ν(O2)=0.36mol•L-1•min-1:若继续通入0.20molYO2和0,.10molO2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36mol<n(YO3)<0.40mol.
(3)V的最简单气态氢化物甲的水溶液显碱性.
一定条件下,甲在恒容密闭容器中发生分解反应(正反应放向为吸热反应)并达平衡后,仅改变下表中反应条件x,下列各项中y随x的增大而增大的是bc.(选填序号).
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时的甲的转化率 |

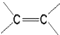 )中的π-键不能自由旋转,因此
)中的π-键不能自由旋转,因此 和
和 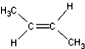 是两种不同的化合物,互为顺反异构体.则分子式为C3H2Cl4的化合物的链状异构体有( )
是两种不同的化合物,互为顺反异构体.则分子式为C3H2Cl4的化合物的链状异构体有( )