题目内容
4.下列离子方程式书写不正确的是( )| A. | 少量铁粉加入稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | H2SO4溶液与Ba(OH)2溶液反应:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O | |
| C. | NaHCO3溶液和过量Ba(OH)2溶液共热:HCO3-+OH-+Ba2+═BaCO3↓+H2O | |
| D. | 苯酚溶液中滴加Na2CO3溶液: +CO32-→HCO3-+ +CO32-→HCO3-+ |
分析 A.铁粉与稀硝酸反应生成硝酸铁和一氧化氮、水;
B.H2SO4溶液与Ba(OH)2溶液反应生成硫酸钡和水;
C.NaHCO3溶液和过量Ba(OH)2溶液共热反应生成碳酸钡和氢氧化钠和水;
D.苯酚与碳酸钠反应生成碳酸氢钠和苯酚钠;
解答 解:A.少量铁粉加入稀硝酸中,生成硝酸亚铁和一氧化氮、水,离子方程式:Fe+4H-+NO3-═Fe3++NO↑+2H2O,故A错误;
B.H2SO4溶液与Ba(OH)2溶液反应,离子方程式:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O,故B正确;
C.NaHCO3溶液和过量Ba(OH)2溶液共热,离子方程式:HCO3-+OH-+Ba2+═BaCO3↓+H2O,故C正确;
D.苯酚溶液中滴加Na2CO3溶液,离子方程式: +CO32-→HCO3-+
+CO32-→HCO3-+ ,故D正确;
,故D正确;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷数守恒规律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.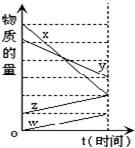 如图表示在某温度下经时间t反应后,物质x、y、z、w的物质的量的变化情况.则所发生反应的化学方程式是( )
如图表示在某温度下经时间t反应后,物质x、y、z、w的物质的量的变化情况.则所发生反应的化学方程式是( )
 如图表示在某温度下经时间t反应后,物质x、y、z、w的物质的量的变化情况.则所发生反应的化学方程式是( )
如图表示在某温度下经时间t反应后,物质x、y、z、w的物质的量的变化情况.则所发生反应的化学方程式是( )| A. | 4x+2y=z+w | B. | 6x+5y=4z+w | C. | 3w+z=4x+2y | D. | 2x+y=2z+2w |
15.下列化合物的核磁共振氢谱中出现三组峰的是( )
| A. | 2,2,3,3-四甲基丁烷 | B. | 3-甲基-1-丁炔 | ||
| C. | 2,3-二甲基-2-戊烯 | D. | 3,3-二乙基戊烷 |
19.据《华盛顿邮报》报道,美国食品与药物管理局2010年2月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A,并不会对婴儿或成人的健康构成威胁.关于双酚A的下列说法相对正确的是( )

| A. | 该化合物属于芳香烃 | |
| B. | 该化合物分子式为C20H24O2 | |
| C. | 1mol双酚A最多消耗4molBr2 | |
| D. | 双酚A能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 |
16.下列化学用语表示正确的是( )
| A. | .甲烷的比例模型: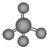 | B. | .氯离子的结构示意图: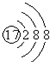 | ||
| C. | CO2分子的电子式: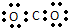 | D. | .中子数为18的硫原子:${\;}_{16}^{34}$S |
13.黄铁矿(主要成分FeS2)、黄铜矿(主要成分CuFeS2)均是自然界中的常见矿物资源.
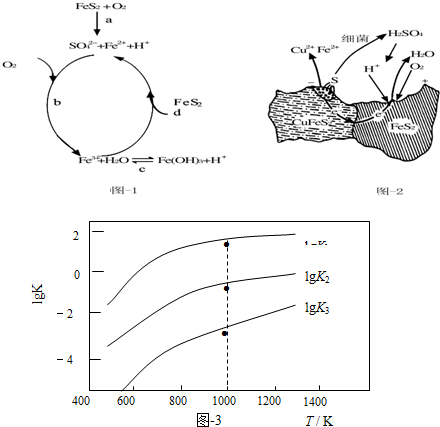
(1)Stumm和Morgan提出黄铁矿在空气中氧化的四步反应如题图-1所示:
①a反应中每生成1molFeSO4转移电子的物质的量为7mol.
②d反应的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+.
(2)用细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高浸取速率,其原理如题图-2
①冶炼过程中,正极周围溶液的pH增大(选填:“增大”、“减小”或“不变”)
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见下表),其相关反应的平衡常数的对数值与温度的关系如题图-3.
①上述反应中,△H1>0(选填:“>”或“<”).
②提高硫的脱除率可采取的措施有升高温度(举1例).
③1000K时,平衡常数的对数lgK1、lgK2和lgK3之间的关系为lgK2=lgK1+lgK3.

(1)Stumm和Morgan提出黄铁矿在空气中氧化的四步反应如题图-1所示:
①a反应中每生成1molFeSO4转移电子的物质的量为7mol.
②d反应的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+.
(2)用细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高浸取速率,其原理如题图-2
①冶炼过程中,正极周围溶液的pH增大(选填:“增大”、“减小”或“不变”)
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见下表),其相关反应的平衡常数的对数值与温度的关系如题图-3.
| 相关反应 | 反应热 | 平衡常数K |
| FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| $\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$Fe(s)+H2S(g) | △H2 | K2 |
| FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(举1例).
③1000K时,平衡常数的对数lgK1、lgK2和lgK3之间的关系为lgK2=lgK1+lgK3.
 ,C、D、E中原子半径最大的为Na.
,C、D、E中原子半径最大的为Na.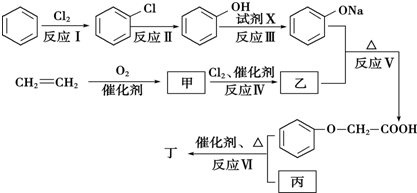
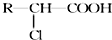
 .
.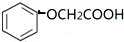 )有多种属于酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且苯环上的一硝基取代物只有两种同分异构体的结构简式有
)有多种属于酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且苯环上的一硝基取代物只有两种同分异构体的结构简式有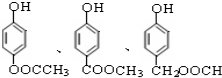 (其中两种)(任写两种即可).
(其中两种)(任写两种即可).


