题目内容
8.五种元素X、Y、Z、W、M在周期表中位置关系如表,其中X、Y、Z、W是短周期元素,Z的气态氢化物与其低价氧化物能反应生成该元素单质的元素.下列说法正确的是( )| X | Y | ||
| Z | W | ||
| M |
| A. | X、Y、Z、W形成的单质中都含有非极性共价键 | |
| B. | 元素最高价氧化物水化物对应的酸性大小W>Z,简单离子半径大小 关系:W>Z>X | |
| C. | M的氢化物的沸点高于X的,化合物M2O3有氧化性和还原性 | |
| D. | 有“海洋元素”美誉的元素与M同周期与W同主族 |
分析 五种元素X、Y、Z、W、M在周期表中位置关系如表,其中X、Y、Z、W是短周期元素,则X、Y位于第二周期,Z、W位于第三周期;Z的气态氢化物与其低价氧化物能反应生成该元素单质的元素,第三周期中S元素的氢化物硫化氢能够与二氧化硫反应生成硫单质,所以Z为S,结合各元素在周期表中的相对位置可知,W为Cl、Y为Ne、X为N、M为As元素,据此结合元素周期律知识解答.
解答 解:五种元素X、Y、Z、W、M在周期表中位置关系如表,其中X、Y、Z、W是短周期元素,则X、Y位于第二周期,Z、W位于第三周期;Z的气态氢化物与其低价氧化物能反应生成该元素单质的元素,第三周期中S元素的氢化物硫化氢能够与二氧化硫反应生成硫单质,所以Z为S,结合各元素在周期表中的相对位置可知,W为Cl、Y为Ne、X为N、M为As元素,
A.Y为Ne,其单质为单原子分子,不存在非极性共价键,故A错误;
B.非金属性W>Z,则元素最高价氧化物水化物对应的酸性大小W>Z;Z为S、W为Cl,氯离子、硫离子具有相同电子层,氯离子的核电荷数较大,其离子半径较小,故B错误;
C.X为N,其氢化物氨气分子中含有氢键,导致其沸点高于AsH3,故C错误;
D.Br是“海洋元素”美誉的元素,Br元素位于第四周期ⅤⅡA族,与As位于同一周期,与Cl位于同一主族,故D正确;
故选D.
点评 本题考查了位置、结构与性质的关系,题目难度不大,推断元素为解答关键,注意熟练掌握元素周期律内容、元素周期表结构,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.具有真正意义上的元素周期表是由哪位化学家发现的是( )
| A. | 门捷列夫(俄国) | B. | 依马林(俄国) | ||
| C. | 别洛索夫(俄国) | D. | 马尔柯夫尼可夫(俄国) |
19.下列各组物质反应后,再滴入KSCN溶液,显红色的是( )
| A. | 向CuCl2溶液中加入铁粉 | |
| B. | 向FeO粉末中加入稀硫酸 | |
| C. | 单质Fe与过量稀盐酸反应后的溶液中再加入少量氯水 | |
| D. | Fe(OH)3与过量稀盐酸反应后的溶液中再加入过量铁粉 |
16.下列离子中半径最小的是( )
| A. | Na+ | B. | F- | C. | Al3+ | D. | O2- |
3.固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图:

根据上述实验,以下说法正确的是( )

根据上述实验,以下说法正确的是( )
| A. | 由现象1和现象3推测溶液甲中一定含有K2SiO3、NaNO2 | |
| B. | 由于在溶液甲中加入足量稀盐酸后再加入BaCl2溶液,因此无法判断溶液中是否有K2SO3 | |
| C. | 无法判断原混合物中是否含有KAlO2、K2CO3、MgCl2 | |
| D. | 根据现象5推测原混合物中一定含有Fe2O3 |
13.离子键和共价键可能同时存在于同一化合物中.下列化合物中既存在离子键又存在共价键的是( )
| A. | KBr | B. | Na2O | C. | HBr | D. | NH4NO3 |
20.下列离子方程式,正确的是( )
| A. | 氯化铝溶液与过量氨水 Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| B. | 明矾净水原理:Al3++3H2O→Al(OH)3↓+3H+ | |
| C. | 将足量氯气通入溴化亚铁溶液:2Fe2++Cl2→2Fe3++2Cl- | |
| D. | 偏铝酸钠溶液与过量盐酸AlO2-+H++H2O→Al(OH)3↓ |
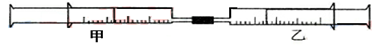
17.如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验.试回答下列问题:
(1)实验1中,沉淀最终变为红褐色,写出沉淀变色的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(2)实验2甲针筒内的现象是:溶液变血红.
(3)实验3中,甲针筒内开始时的现象是:白色沉淀;若甲针筒内产生的沉淀的质量为0.39g,则则需向甲针筒内注入该NaOH溶液15 mL或35mL.
(4)实验4中,若持续向甲针筒内注入1mol/LBa(OH)2溶液,当生成沉淀的物质的量最大时,沉淀成分为BaSO4和Al(OH)3.(填化学式,下同).当生成沉淀的质量最大时,沉淀成分为BaSO4.

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 10mL FeSO4溶液 | 10mLNH3 | 生成白色沉淀,后变色 |
| 2 | 5mL1mol/L FeCl3溶液 | 1mL1mol/L KSCN溶液 | |
| 3 | 10mL1mol/LAlCl3溶液 | 1mol/L NaOH | |
| 4 | 10mL2mol/LKAl(SO4)2溶液 | 1mol/LBa(OH)2溶液 |
(2)实验2甲针筒内的现象是:溶液变血红.
(3)实验3中,甲针筒内开始时的现象是:白色沉淀;若甲针筒内产生的沉淀的质量为0.39g,则则需向甲针筒内注入该NaOH溶液15 mL或35mL.
(4)实验4中,若持续向甲针筒内注入1mol/LBa(OH)2溶液,当生成沉淀的物质的量最大时,沉淀成分为BaSO4和Al(OH)3.(填化学式,下同).当生成沉淀的质量最大时,沉淀成分为BaSO4.
19.已知:4P(红磷,S)═P4(白磷,s)△H=+17kJ•moL-1,则下列推论正确的是( )
| A. | 当1 mol白磷完全转变成红磷时放出17kJ热量 | |
| B. | 正反应是一个放热反应 | |
| C. | 当4g红磷转变成白磷时吸收I7k J热量 | |
| D. | 白磷比红磷稳定 |