题目内容
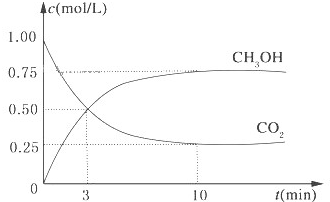 降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.
降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
(2)氢气的转化率=
(3)该反应的平衡常数为
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去
D.再充入1mol H2
(5)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1
考点:物质的量或浓度随时间的变化曲线,化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:(1)根据v=
计算;
(2)根据氢气的平衡浓度判断转化的物质的量,进而可计算转化率;
(3)根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积计算;
(4)要使n(CH3OH)/n(CO2)增大,应使平衡向正反应方向移动;
(5)恒容密闭容器、反应后整个体系的压强比之前来说减小了,加入氢气虽然正向移动,但是CO2(g)浓度较小、CH3OH(g) 浓度增大、H2O(g)浓度增大,且平衡常数不变.
| △c |
| △t |
(2)根据氢气的平衡浓度判断转化的物质的量,进而可计算转化率;
(3)根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积计算;
(4)要使n(CH3OH)/n(CO2)增大,应使平衡向正反应方向移动;
(5)恒容密闭容器、反应后整个体系的压强比之前来说减小了,加入氢气虽然正向移动,但是CO2(g)浓度较小、CH3OH(g) 浓度增大、H2O(g)浓度增大,且平衡常数不变.
解答:
解:(1)利用三段式解题法计算
CO2(g)+3H2(g) CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g),
开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
从反应开始到平衡,氢气的平均反应速率v(H2)=
=0.225 mol?L-1?min-1,
故答案为:0.225;
(2)氢气的转化率=
=75%,
故答案为:75%;
(3)平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,则k=
=
=5.33,
故答案为:5.33;
(4)要使n(CH3OH)/n(CO2)增大,应使平衡向正反应方向移动,
A.因正反应放热,升高温度平衡向逆反应方向移动,则n(CH3OH)/n(CO2)减小,故A错误;
B.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,n(CH3OH)/n(CO2)不变,故D错误.故B错误;
C.将H2O(g)从体系中分离,平衡向正反应方法移动,n(CH3OH)/n(CO2)增大,故C正确;
D.再充入1mol H2,增大反应物浓度,平衡向正反应方向移动,则n(CH3OH)/n(CO2)增大,故D正确.
故答案为:CD;
(5)若是恒容密闭容器、反应后整个体系的压强比之前来说减小了,加入氢气虽然正向移动,平衡移动的结果是减弱这种改变,而不能消除这种改变,即虽然平衡正向移动,氢气的物质的量在增加后的基础上减小,但是CO2(g)浓度较小、CH3OH(g) 浓度增大、H2O(g)浓度增大,且平衡常数不变达到平衡时H2的物质的量浓度与加氢气之前相比一定增大,故c1<c2,故答案为:<.
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g),开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
从反应开始到平衡,氢气的平均反应速率v(H2)=
| 2.25mol/L |
| 10min |
故答案为:0.225;
(2)氢气的转化率=
| 2.25 |
| 3 |
故答案为:75%;
(3)平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,则k=
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
| 0.75×0.75 |
| 0.25×0.753 |
故答案为:5.33;
(4)要使n(CH3OH)/n(CO2)增大,应使平衡向正反应方向移动,
A.因正反应放热,升高温度平衡向逆反应方向移动,则n(CH3OH)/n(CO2)减小,故A错误;
B.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,n(CH3OH)/n(CO2)不变,故D错误.故B错误;
C.将H2O(g)从体系中分离,平衡向正反应方法移动,n(CH3OH)/n(CO2)增大,故C正确;
D.再充入1mol H2,增大反应物浓度,平衡向正反应方向移动,则n(CH3OH)/n(CO2)增大,故D正确.
故答案为:CD;
(5)若是恒容密闭容器、反应后整个体系的压强比之前来说减小了,加入氢气虽然正向移动,平衡移动的结果是减弱这种改变,而不能消除这种改变,即虽然平衡正向移动,氢气的物质的量在增加后的基础上减小,但是CO2(g)浓度较小、CH3OH(g) 浓度增大、H2O(g)浓度增大,且平衡常数不变达到平衡时H2的物质的量浓度与加氢气之前相比一定增大,故c1<c2,故答案为:<.
点评:本题考查较为综合,涉及化学平衡计算以及平衡移动等问题,题目难度较大,注意根据图象计算各物质的平衡浓度为解答该题的关键.

练习册系列答案
相关题目
同温同压下,1molHe和1molH2具有相同的( )
| A、原子数 | B、质量 |
| C、中子数 | D、体积 |
类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列说法正确的是( )
| A、CaC2能水解:CaC2+2H2O═Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O═4Al(OH)3↓+3CH4↑ |
| B、O2与Cu加热反应生成CuO,则S与Cu加热反应生成CuS |
| C、根据化合价Fe3O4可表示为FeO?Fe2O3,则Fe3I8也可表示为FeI2?2FeI3 |
| D、SO2通入BaCl2溶液中不产生沉淀,则SO2通入Ba(NO3)2溶液中也不产生沉淀 |
羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得:

下列有关说法正确的是( )

下列有关说法正确的是( )
| A、苯酚和羟基扁桃酸互为同系物 |
| B、羟基扁桃酸分子中至少有12个原子共平面 |
| C、乙醛酸在核磁共振氢谱中只有1个吸收峰 |
| D、常温下,1 mol羟基扁桃酸只能与1 mol Br2反应 |
 某化学兴趣小组利用下图装置测定某硫酸工厂排放尾气中二氧化硫的含量,图中气体流量计B用于准确测量通过的尾气体积.将尾气通入一定体积已知浓度的碘水中测定SO2的含量.当洗气瓶C中溶液蓝色消失时,立即关闭活塞A.
某化学兴趣小组利用下图装置测定某硫酸工厂排放尾气中二氧化硫的含量,图中气体流量计B用于准确测量通过的尾气体积.将尾气通入一定体积已知浓度的碘水中测定SO2的含量.当洗气瓶C中溶液蓝色消失时,立即关闭活塞A. 已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.回答下列问题:
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.回答下列问题: