题目内容
下列各溶液中,pH最大的是( )
| A、pH=9的氨水溶液稀释1000倍 |
| B、pH=9的烧碱溶液稀释1000倍 |
| C、pH=5的盐酸溶液稀释1000倍 |
| D、pH=5的氯化铵溶液稀释1000倍 |
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:A.氨水是弱碱,稀释1000倍,溶液几乎变为中性,但仍为碱溶液PH略大于7;
B.溶液中的离子积Kw=c(H+)×c(OH-),pH=9的烧碱溶液稀释1000倍,溶液几乎变为中性,但仍为碱溶液PH略大于7;
C.pH=5的盐酸溶液稀释1000倍,稀释后溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液;
D.氯化铵电离的铵根离子水解,溶液显示酸性,稀释后溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液.
B.溶液中的离子积Kw=c(H+)×c(OH-),pH=9的烧碱溶液稀释1000倍,溶液几乎变为中性,但仍为碱溶液PH略大于7;
C.pH=5的盐酸溶液稀释1000倍,稀释后溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液;
D.氯化铵电离的铵根离子水解,溶液显示酸性,稀释后溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液.
解答:
解:A.氨水是弱碱,稀释1000倍,此时水的电离占了主要地位,溶液几乎变为中性,但仍为碱溶液pH略大于7;
B.常温下,溶液中的离子积Kw=c(H+)×c(OH-)=10-14,pH=9的NaOH中c(OH-)=10-5mol/L,稀释1000倍,此时水的电离占了主要地位,溶液中的c(H+)≈10-7mol/L,溶液几乎变为中性,但仍为碱溶液pH略大于7;
C.pH=5的盐酸中氢离子浓度为c(H+)=10-5mol/L,溶液稀释1000倍后,溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液;
D.pH=5的氯化铵溶液中c(H+)=10-5mol/L,稀释1000倍后溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液;
pH=9的氨水稀释1000倍,与pH=9的烧碱溶液稀释1000倍相比,稀释相同的倍数时,氨水是弱电解质,pH变化程度小,所以稀释后溶液的pH:A>B;C中pH小于7、D中pH小于7,
所以pH最大的为A,
故选A.
B.常温下,溶液中的离子积Kw=c(H+)×c(OH-)=10-14,pH=9的NaOH中c(OH-)=10-5mol/L,稀释1000倍,此时水的电离占了主要地位,溶液中的c(H+)≈10-7mol/L,溶液几乎变为中性,但仍为碱溶液pH略大于7;
C.pH=5的盐酸中氢离子浓度为c(H+)=10-5mol/L,溶液稀释1000倍后,溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液;
D.pH=5的氯化铵溶液中c(H+)=10-5mol/L,稀释1000倍后溶液中c(H+)≈10-7mol/L,但仍然为酸性溶液;
pH=9的氨水稀释1000倍,与pH=9的烧碱溶液稀释1000倍相比,稀释相同的倍数时,氨水是弱电解质,pH变化程度小,所以稀释后溶液的pH:A>B;C中pH小于7、D中pH小于7,
所以pH最大的为A,
故选A.
点评:本题考查酸碱溶液稀释后的溶液中pH的判断,题目难度中等,注意酸碱电解质的强弱以及盐类水解的酸碱性,特别是pH与溶液稀释后的酸碱性关系.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
下列物质的电子式,正确的是( )
A、 |
B、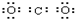 |
C、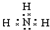 |
D、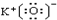 |
将羧酸的碱金属盐电解可生成烃类化合物,例如:2CH3COOK+2H2O
CH3-CH3↑+2CO2↑+H2↑+2KOH
现充分电解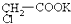 水溶液,并加热电解后的水溶液,则下列说法中合理的是( )
水溶液,并加热电解后的水溶液,则下列说法中合理的是( )
| ||
现充分电解
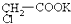 水溶液,并加热电解后的水溶液,则下列说法中合理的是( )
水溶液,并加热电解后的水溶液,则下列说法中合理的是( )| A、CO2气体在阴极放出 |
| B、加热后有不溶于水的油状物生成 |
| C、混合液蒸干后得到的固体物质是KOH |
| D、混合液蒸干后得到的固体物质是KCl |
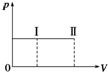 一带有活塞的绝热密闭容器中盛有A、B组成的混合气体,并发生如下反应:A(g)+B(g)?2C(g),在通常条件下,反应从状态Ⅰ变化到状态Ⅱ时,气体体积(V)与气体压强(p)的变化曲线如图所示.则下列说法正确的是( )
一带有活塞的绝热密闭容器中盛有A、B组成的混合气体,并发生如下反应:A(g)+B(g)?2C(g),在通常条件下,反应从状态Ⅰ变化到状态Ⅱ时,气体体积(V)与气体压强(p)的变化曲线如图所示.则下列说法正确的是( )| A、反应物具有的总能量等于生成物具有的总能量 |
| B、反应从状态Ⅰ变化到状态Ⅱ时,混合气体的平均相对分子质量减小 |
| C、反应从状态Ⅰ变化到状态Ⅱ时,反应速率一定减小 |
| D、该反应是放热反应 |
化学与生产、生活密切相关,下列有关叙述正确的是( )
| A、晶体硅是“信息革命“的支柱材料,可用作光导纤维 |
| B、将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| C、化学反应伴随着能量的变化,反应物总能量一定大于生成物总能量 |
| D、用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 |