题目内容
7.已知某气体单质R3的摩尔质量为M g•mol-1,阿伏加德罗常数的数值用NA表示,现有V L(标准状况下)该气体,用含M、V、NA的代数式回答下列问题:(1)该气体的物质的量为$\frac{V}{22.4}$mol.
(2)该气体在标准状况下的密度为$\frac{M}{22.4}$g•L-1.
(3)该气体所含原子总数为$\frac{3V{N}_{A}}{22.4}$.
(4)一个R原子的质量为$\frac{M}{3{N}_{A}}$g.
分析 (1)V L(标准状况下)该气体物质的量n=$\frac{V}{22.4}$mol;
(2)气体单质R3的摩尔质量为M g•mol-1,该气体在标准状况下,带入M=22.4ρ计算;
(3)气体单质R3的摩尔质量为M g•mol-1,该气体物质的量n=$\frac{V}{22.4}$mol,n=$\frac{N}{{N}_{A}}$计算原子总数;
(4)气体单质R3的摩尔质量为M g•mol-1,即NA个分子质量为Mg.
解答 解:(1)V L标准状况下该气体依据其他摩尔体积计算气体物质的量n=$\frac{V}{22.4}$mol,
故答案为:$\frac{V}{22.4}$;
(2)气体单质R3的摩尔质量为M g•mol-1,该气体在标准状况下,带入M=22.4ρ计算得到ρ=$\frac{M}{22.4}$g/L,
故答案为:$\frac{M}{22.4}$;
(3)气体单质R3的摩尔质量为M g•mol-1,该气体物质的量n=$\frac{V}{22.4}$mol,n=$\frac{N}{{N}_{A}}$计算原子总数,N=$\frac{V}{22.4}$×3×NA=$\frac{3V{N}_{A}}{22.4}$
故答案为:$\frac{3V{N}_{A}}{22.4}$;
(4)气体单质R3的摩尔质量为M g•mol-1,即NA个分子质量为Mg,一个R原子的质量=$\frac{M}{3{N}_{A}}$g,
故答案为:$\frac{M}{3{N}_{A}}$.
点评 本题考查物质的量的相关计算,题目难度中等,综合性较强,充分考查学生的分析、理解能力及灵活应用公式的能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
17.某混合烃有甲烷和乙烯组成,将2L该混合烃燃烧后得2.8L CO2和4L水蒸汽,则该混合烃中,甲烷和乙烯的体积比为( )
| A. | 2:3 | B. | 3:2 | C. | 1:4 | D. | 4:1 |
18.下列关于SO2的说法中,不正确的是( )
| A. | SO2是硫及某些含硫化合物在空气中燃烧的产物 | |
| B. | SO2具有漂白性,可以使品红溶液褪色 | |
| C. | SO2溶于水后生成H2SO4 | |
| D. | SO2是一种大气污染物 |
15.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、电子天平、药匙、量筒、玻璃棒、500 mL容量瓶、胶头滴管.(在横线上填写所缺仪器的名称)
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.25 | 174 |
| 阿司匹林(C9H8O4) | 0.17 | 180 |
| 高锰酸钾 | 0.25 | 158 |
| 硝酸银 | 0.02 | 170 |
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
12.下列反应中,调节反应物的用量或浓度以后,不会改变反应产物的是( )
| A. | 酒精在氧气中燃烧 | B. | 在硫酸中加入铝粉 | ||
| C. | 将二氧化碳气体通入烧碱中 | D. | 向盐酸中加入铁钉 |
3.某温度下,反应2N2O5(g)═4NO2(g)+O2(g)开始时,c(N2O5)=0.040 8mol•L-1,经1min后,c(N2O5)=0.030 0mol•L-1.则该反应的反应速率为( )
| A. | v(N2O5)=1.80×10-3 mol•L-1•min-1 | B. | v(N2O5)=1.08×10-2 mol•L-1•min-1 | ||
| C. | v(NO2)=1.80×10-3 mol•L-1•min-1 | D. | v(O2)=1.80×10-2 mol•L-1•min-1 |
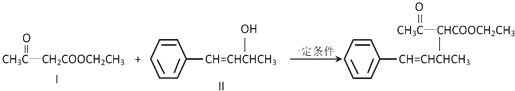
 .
.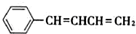 .
.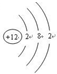 .
. .
.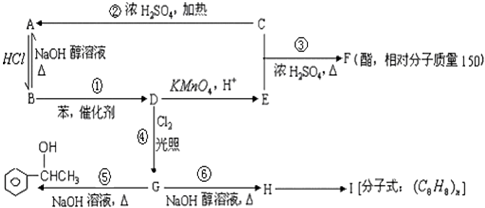
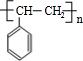
 ;③
;③ +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O;⑥
+H2O;⑥ .
.