题目内容
 实验室制取乙烯:C2H5OH
实验室制取乙烯:C2H5OH | 170℃ |
| 浓硫酸 |
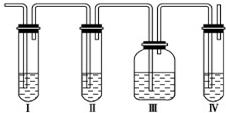
(1)各装置盛放的试剂是:Ⅰ
A.NaOH 溶液
B.品红溶液
C.浓H2SO4溶液
D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
(3)使用装置Ⅱ的目的是
(4)确认含乙烯的现象是
考点:物质的检验和鉴别的实验方案设计,乙烯的化学性质
专题:实验设计题
分析:二氧化硫的检验用品红溶液,乙烯的检验用高锰酸钾酸性溶液,乙烯和二氧化硫都能使高锰酸钾酸性溶液褪色,所以先检验二氧化硫,然后检验乙烯,同在检验乙烯之前用NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用高锰酸钾酸性溶液褪色检验乙烯,据此回答问题.
解答:
解:(1)因装置Ⅰ用来检验SO2,试管中品红溶液褪色,说明含有SO2,装置Ⅱ试管装有NaOH溶液除去SO2,装置Ⅲ通过品红溶液不褪色确认SO2已除干净,装置Ⅳ通过高锰酸钾酸性溶液褪色检验乙烯,
故答案为:B、A、B、D;
(2)装置Ⅰ用来检验SO2,试管中品红溶液褪色,说明含有SO2,
故答案为:Ⅰ中品红溶液褪色;
(3)装置Ⅱ试管装有NaOH溶液除去SO2,以免干扰乙烯的检验;装置Ⅲ通过品红溶液不褪色确认SO2已除干净,
故答案为:除去SO2,以免干扰乙烯的检验;确认SO2已除干净;
(4)装置Ⅳ通过高锰酸钾酸性溶液褪色检验乙烯,确认含乙烯的现象是:Ⅲ中溶液不褪色,Ⅳ中高锰酸钾酸性溶液褪色,
故答案为:Ⅲ中溶液不褪色,Ⅳ中高锰酸钾酸性溶液褪色.
故答案为:B、A、B、D;
(2)装置Ⅰ用来检验SO2,试管中品红溶液褪色,说明含有SO2,
故答案为:Ⅰ中品红溶液褪色;
(3)装置Ⅱ试管装有NaOH溶液除去SO2,以免干扰乙烯的检验;装置Ⅲ通过品红溶液不褪色确认SO2已除干净,
故答案为:除去SO2,以免干扰乙烯的检验;确认SO2已除干净;
(4)装置Ⅳ通过高锰酸钾酸性溶液褪色检验乙烯,确认含乙烯的现象是:Ⅲ中溶液不褪色,Ⅳ中高锰酸钾酸性溶液褪色,
故答案为:Ⅲ中溶液不褪色,Ⅳ中高锰酸钾酸性溶液褪色.
点评:本题主要考查了实验室制乙烯产物的检验,当有多种产物需检验时,应考虑先后顺序,在除去杂质气体时不能引入新杂质,本题难度中等.

练习册系列答案
相关题目
某有机物甲经水解可得乙,乙在一定条件下经氧化后可得丙,1mol丙和2mol甲反应得一种含氯的酯(C6H8O4Cl2).由此推断有机物丙的结构简式为( )
A、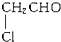 |
| B、HOCH2CH2OH |
C、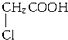 |
D、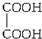 |
对③装置叙述正确的是( )
| A、Fe作正极,Zn作负极 |
| B、Fe处发生的反应为:Fe+Cu2+═Fe2++Cu |
| C、Fe作负极,Zn作正极 |
| D、Zn处发生的反应为:Zn+Cu2+═Zn2++Cu |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A、标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为
| ||
| B、1 mol甲基(-CH3)所含的电子总数为10NA | ||
| C、7 g CnH2n中含有的氢原子数目为NA | ||
| D、1mol金刚石晶体中,平均含有碳碳单键键数为4 NA |
下列关于原电池的叙述正确的是( )
| A、构成原电池的正极和负极必须是两种不同的金属 |
| B、原电池是将化学能转变为电能的装置 |
| C、原电池中电子流出的一极是负极,该极被还原 |
| D、原电池放电时,电流的方向是从负极到正极 |
在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是( )
| A、NaOH |
| B、NH3?H2O |
| C、AgNO3 |
| D、BaCl2 |
对如图所示分子的描述不正确的是( )
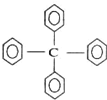

| A、该物质的分子式为C25H20 |
| B、该物质所有氢原子不可能在同一平面上 |
| C、该物质属于烷烃 |
| D、该物质的一氯代物有3种 |