题目内容
 SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一.
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一.(1)在接触法制硫酸的过程中,发生2SO2(g)+O2(g)
| 催化剂 |
| △ |
①平衡状态由A到B时,平衡常数K(A)
②将2.0molSO2和1.0molO2置于10L的密闭容器中,若40s后反应达到平衡,此时体系总压强为0.10MPa,这一段时间内SO2的平均反应速率为
(2)用CH4催化还原NOx可消除氮的氧化物的污染,例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
取标准状况下4.48LCH4并使之完全反应:
①若将NO2还原至N2,整个过程中转移电子的物质的量为
②若还原NO2和NO的混合物,放出的总热量Q的取值范围是
考点:化学平衡的计算,化学平衡常数的含义,转化率随温度、压强的变化曲线
专题:化学平衡专题
分析:(1)①根据平衡常数只受温度的影响判断;
②由图象可知压强为0.10MPa时SO2的为80%,计算各物质的平衡浓度,可计算反应速率和平衡常数;
(2)已知①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ/mol
利用盖斯定律将
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g),以此计算反应热,结合元素的化合价变化计算转移的电子数.
②由图象可知压强为0.10MPa时SO2的为80%,计算各物质的平衡浓度,可计算反应速率和平衡常数;
(2)已知①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ/mol
利用盖斯定律将
| ①+② |
| 2 |
解答:
解:(1)平衡常数只受温度的影响,温度不变,则压强不变,平衡状态由A变到B时,则k(A)=k(B),故答案为:①=;
②由图象知,体系总压强为0.10MPa时SO2的平衡转化率为0.8,则
2SO2(g)+O2(g)
2SO3(g)
起始:2.0mol 1.0mol 0
转化:1.6mol 0.8mol 1.6mol
平衡:0.4mol 0.2mol 1.6mol
则v(SO2)=
=0.0040mol?L-1?s-1,
则平衡时:c(SO2)=0.04mol/L,c(O2)=0.02mol/L,c(SO3)=0.16mol/L,
K=
=
=800,
故答案为:0.0040mol?L-1?s-1;800L?mol-1;
(1)①已知①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ/mol
利用盖斯定律将
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol,
n(CH4)=
=0.2mol,
整个过程中转移的电子总数为:0.20mol×8mol=1.60mol,
故答案为:1.6mol;
②若全部为NO,则发生CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1,放出的热量为0.2mol×1160kJ?mol-1=232kJ,
若全部为NO2,则发生CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ/mol,放出的热量为0.2mol×867kJ/mol=173.4kJ,
则放出的总热量Q的取值范围是173.4kJ<Q<232kJ,
故答案为:173.4kJ<Q<232kJ.
②由图象知,体系总压强为0.10MPa时SO2的平衡转化率为0.8,则
2SO2(g)+O2(g)
| 催化剂 |
| △ |
起始:2.0mol 1.0mol 0
转化:1.6mol 0.8mol 1.6mol
平衡:0.4mol 0.2mol 1.6mol
则v(SO2)=
| ||
| 40s |
则平衡时:c(SO2)=0.04mol/L,c(O2)=0.02mol/L,c(SO3)=0.16mol/L,
K=
| c2(SO3) |
| c2(SO2)?c(O2) |
| (0.16)2 |
| (0.04)2×0.02 |
故答案为:0.0040mol?L-1?s-1;800L?mol-1;
(1)①已知①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ/mol
利用盖斯定律将
| ①+② |
| 2 |
n(CH4)=
| 4.48L |
| 22.4L/mol |
整个过程中转移的电子总数为:0.20mol×8mol=1.60mol,
故答案为:1.6mol;
②若全部为NO,则发生CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1,放出的热量为0.2mol×1160kJ?mol-1=232kJ,
若全部为NO2,则发生CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ/mol,放出的热量为0.2mol×867kJ/mol=173.4kJ,
则放出的总热量Q的取值范围是173.4kJ<Q<232kJ,
故答案为:173.4kJ<Q<232kJ.
点评:本题考查化学平衡及化学反应及能量,侧重于学生的分析能力和计算能力的考查,为高频考点,题目难度中等,本题易错点为化学平衡常数的计算,注意计算过程的把握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
两种盐的固体混合物:①加热时有气体产生,②加水溶解时有沉淀生成,且沉淀溶于稀盐酸.满足上述条件的混合物是( )
| A、BaCl2 和(NH4)2C03 |
| B、AgNO3 和 NH4Cl |
| C、FeCl3和 NaHCO3 |
| D、KCl 和 Na2CO3 |
某温度下,反应2A(g)?B(g)(正反应为放热反应),在密闭容器中达到平衡,平衡后
=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时
=b,下列叙述不正确的是( )
| c(A) |
| c(B) |
| c(A) |
| c(B) |
| A、在该温度下,保持容积固定不变,向容器内补充了B气体,则a>b |
| B、保持温度、压强不变,充入惰性气体,则有a<b |
| C、若其他条件不变,升高温度,则有a<b |
| D、若a=b,容器中一定使用了催化剂 |
常温下,某溶液中由水电离产生的c(H+)、c(OH-)满足c(H+)?c(OH-)=10-26,则下列各组离子在该溶液中一定可以大量共存的是( )
| A、K+、Na+、AlO2-、Cl- |
| B、Na+、Cl-、SO42-、HCO3- |
| C、NH4+、Fe3+、NO3-、SO42- |
| D、Ba2+、Na+、Cl-、NO3- |
 已知下列反应(反应所需的条件、反应物的浓度和方程式中各物质的化学计量数均已略去):
已知下列反应(反应所需的条件、反应物的浓度和方程式中各物质的化学计量数均已略去):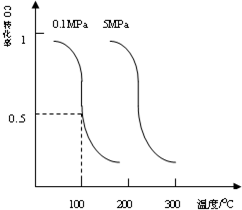 研究和开发CO2和CO的创新利用是环境保护和资源利用的双赢的课题.
研究和开发CO2和CO的创新利用是环境保护和资源利用的双赢的课题. 为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果如图.CO转化率随温度变化的规律是
为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果如图.CO转化率随温度变化的规律是 某学生用电子天平和必要的化学实验仪器测定铁铝合金中各组分含量,其实验装置如图所示:实验时,取一块铁铝合金,将其切成碎块后全部加入到盛有50mL 5.0mol?L-1 NaOH溶液的烧杯中.试回答下列问题:
某学生用电子天平和必要的化学实验仪器测定铁铝合金中各组分含量,其实验装置如图所示:实验时,取一块铁铝合金,将其切成碎块后全部加入到盛有50mL 5.0mol?L-1 NaOH溶液的烧杯中.试回答下列问题: