题目内容
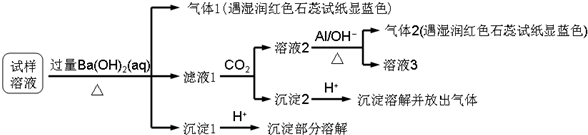
雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.某同学收集了该地区的雾霾,经必要的预处理后的试样溶液,设计并完成了如下实验:
已知:3NO3-+8Al+5OH-+2H2O
3NH3↑+8AlO2-
根据以上的实验操作和现象,该同学得出的结论不正确的是( )

已知:3NO3-+8Al+5OH-+2H2O
| △ |
根据以上的实验操作和现象,该同学得出的结论不正确的是( )
| A、试样中肯定存在NH4+、Mg2+、SO42-和NO3- |
| B、试样中一定不含Al3+ |
| C、试样中可能存在Na+、Cl- |
| D、该雾霾中可能存在NaNO3、NH4Cl和MgSO4 |
考点:真题集萃,常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:试样溶液中加入过量Ba(OH)2并加热,生成的气体1能使湿润的红色石蕊试纸变蓝色,说明气体1是NH3,则试样中含有NH4+;
向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,生成气体2,该气体能使湿润红色石蕊试纸变蓝色,说明含有气体2是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;
滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐;
沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg 2+,结合题给选项分析解答.
向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,生成气体2,该气体能使湿润红色石蕊试纸变蓝色,说明含有气体2是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;
滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐;
沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg 2+,结合题给选项分析解答.
解答:
解:试样溶液中加入过量Ba(OH)2并加热,生成的气体1能使湿润的红色石蕊试纸变蓝色,说明气体1是NH3,则试样中含有NH4+;
向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,生成气体2,该气体能使湿润红色石蕊试纸变蓝色,说明含有气体2是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;
滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐,也有可能是试样中存在Al3+,在过量的Ba(OH)2中反应生成AlO2-,通入CO2后生成Al(OH)3沉淀;
沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,以及能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg 2+,
A.通过以上分析知,试样中肯定存在NH4+、Mg2+、SO42-和NO3-,故A正确;
B.通过以上分析知,试样中不能确定是否含有Al3+,故B错误;
C.通过以上分析知,试样中可能存在Na+、Cl-,故C正确;
D.根据以上分析知,试样中肯定存在NH4+、Mg2+、SO42-和NO3-,可能存在Na+、Cl-,所以该雾霾中可能存在NaNO3、NH4Cl和MgSO4,故D正确;
故选B.
向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,生成气体2,该气体能使湿润红色石蕊试纸变蓝色,说明含有气体2是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;
滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐,也有可能是试样中存在Al3+,在过量的Ba(OH)2中反应生成AlO2-,通入CO2后生成Al(OH)3沉淀;
沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,以及能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg 2+,
A.通过以上分析知,试样中肯定存在NH4+、Mg2+、SO42-和NO3-,故A正确;
B.通过以上分析知,试样中不能确定是否含有Al3+,故B错误;
C.通过以上分析知,试样中可能存在Na+、Cl-,故C正确;
D.根据以上分析知,试样中肯定存在NH4+、Mg2+、SO42-和NO3-,可能存在Na+、Cl-,所以该雾霾中可能存在NaNO3、NH4Cl和MgSO4,故D正确;
故选B.
点评:本题考查了物质的推断,明确物质的性质及特殊反应现象是解本题关键,根据物质的溶解性、物质的性质及题给信息来分析解答,题目难度中等.

练习册系列答案
相关题目
一定温度下,向饱和Na2SO4溶液中加入ag无水Na2SO4粉末,搅拌、静置后析出bgNa2SO4?10H2O晶体,则bg-ag的值是( )
| A、原饱和溶液中减少的Na2SO4的质量 |
| B、原饱和溶液中失去的水的质量 |
| C、原饱和溶液中失去的水和NaSO4的质量总和 |
| D、析出晶体中含有的Na2SO4的质量 |
下列所述变化规律正确的是( )
| A、Na、Mg、Al还原性依次增强 |
| B、HCl、PH3、H2S稳定性依次减弱 |
| C、LiOH、NaOH、KOH碱性依次减弱 |
| D、O2-、F-、Na+、Mg2+的离子半径依次减小 |
 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A、该反应的化学方程式为3B+4D?6A+2C |
| B、反应进行到1s时,v(A)=v(D) |
| C、反应进行到6s时,各物质的百分含量不变 |
| D、反应进行到6s时,B的平均反应速率为0.05mol/(L?min) |
下列有关溶液组成的描述合理的是( )
| A、无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- |
| B、酸性溶液中可能大量存在Na+、ClO-、SO42-、I- |
| C、弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
| D、中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- |
已知某温度下CH3COOH和NH3?H2O的电离常数相等,现向10mL浓度为0.1mol?L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
| A、水的电离程度始终增大 | ||
B、
| ||
| C、c(CH3COOH)与c(CH3COO-)之和始终保持不变 | ||
| D、当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-) |
构成SiO2的化学键在性质上和构成CO2分子的共价键都是极性键,所以( )
| A、SiO2和CO2都属于原子晶体 |
| B、SiO2和CO2都是分子晶体 |
| C、前者是原子晶体,后者是分子晶体 |
| D、前者是分子晶体,后者是原子晶体 |