题目内容
6.甲醇燃料分为甲醇汽油和甲醇柴油,工业合成甲醇的方法很多.(1)一定条件下发生反应:
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1
2CO(g)+O2(g)═2CO2(g)△H2
2H2(g)+O2(g)═2H2O(g)△H3
则CO(g)+2H2(g)?CH3OH(g)的△H═△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3.
(2)在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)与反应时间t的变化曲线如图1所示,该反应的△H<0 (填>、<或=).
(3)若要提高甲醇的产率,可采取的措施有(填字母)ABE
A.缩小容器体积 B.降低温度 C.升高温度
D.使用合适的催化剂 E.将甲醇从混合体系中分离出来

(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,计算该温度下上述反应的化学平衡常数6.75(结果保留小数点后两位数字)
(5)以甲醇为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,图2是目前研究较多的一类固体氧化物燃料电池工作原理示意图,B极的电极反应式为CH3OH+3O2--6e-=CO2+2H2O
(6)25℃时,草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9.向10ml碳酸钙的饱和溶液中逐滴加入8.0×10-4mol•L-1的草酸钾溶液10ml,能否产生沉淀否(填“能”或“否”).
分析 (1)①CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1
②2CO(g)+O2(g)=2CO2(g)△H2
③2H2(g)+O2(g)=2H2O(g)△H3
由盖斯定律可知,①+②×$\frac{1}{2}$-③×$\frac{1}{2}$得CO(g)+2H2(g)?CH3OH(g);
(2)在300℃到500℃时,物质的量n(CH3OH)减小,平衡逆向移动,逆反应是吸热反应;
(3)A.缩小容器体积,增大压强,平衡正向移动;
B.该反应为放热反应,降低温度,平衡正向移动;
C.升高温度,平衡逆向移动;
D.催化剂不影响平衡移动;
E.将甲醇从混合体系中分离出来,生成物浓度减小,平衡正向移动;
(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1molCH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,
CH4+H2O?CO+3H2
起始物质的量浓度(mol•L-1) 1.0 1.0 0 0
转化物质的量浓度(mol•L-1) 0.5 0.5 0.5 1.5
平衡物质的量浓度(mol•L-1 0.5 0.5 0.5 1.5
结合平衡浓度计算K;
(5)负极上甲醇失电子生成二氧化碳;
(6)碳酸钙溶液中钙离子浓度为$\sqrt{2.5×1{0}^{-9}}$mol/L=5×10-5mol/L,二者混合后,钙离子浓度=2.5×10-5mol/L,草酸钾浓度为4.0×10-4mol/L,结合Qc与Ksp判断.
解答 解:(1)①CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1
②2CO(g)+O2(g)=2CO2(g)△H2
③2H2(g)+O2(g)=2H2O(g)△H3
由盖斯定律可知,①+②×$\frac{1}{2}$-③×$\frac{1}{2}$得CO(g)+2H2(g)?CH3OH(g),则△H=△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3,
故答案为:△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3;
(2)在300℃到500℃时,物质的量n(CH3OH)减小,平衡逆向移动,逆反应是吸热反应,正反应是放热反应,即△H<0,
故答案为:<;
(3)A.缩小容器体积,增大压强,平衡正向移动,甲醇的产率增加,故正确;
B.降低温度,平衡正向移动,甲醇的产率增加,故正确;
C.升高温度,平衡逆向移动,甲醇的产率减少,故错误;
D.使用合适的催化剂,平衡不移动,故错误;
E.将甲醇从混合体系中分离出来,有利平衡正向移动,提高甲醇的产量,故正确;
故答案为:A B E;
(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1molCH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,
CH4+H2O?CO+3H2
起始物质的量浓度(mol•L-1) 1.0 1.0 0 0
转化物质的量浓度(mol•L-1) 0.5 0.5 0.5 1.5
平衡物质的量浓度(mol•L-1 0.5 0.5 0.5 1.5
K=$\frac{0.5×1.{5}^{3}}{0.5×0.5}$=6.75mol2/L2,
故答案为:6.75;
(5)由原电池原理可知,负极上甲醇失电子生成二氧化碳,电极反应为CH3OH+3O2--6e-=CO2+2H2O,
故答案为:CH3OH+3O2--6e-=CO2+2H2O;
(6)碳酸钙溶液中钙离子浓度为$\sqrt{2.5×1{0}^{-9}}$mol/L=5×10-5mol/L,二者混合后,钙离子浓度=2.5×10-5mol/L,草酸钾浓度为4.0×10-4mol/L,混合后c(Ca2+)•c(C2O42-)=2.5×10-5×4.0×10-4=1×10-8<Ksp(4.0×10-8),故无沉淀,
故答案为:否.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、平衡移动、电极反应、沉淀生成、盖斯定律应用为解答的关键,侧重分析与计算能力的考查,注意利用平衡浓度计算K,综合性较强,题目难度中等.

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案Ⅰ.若在20L的密闭容器中按物质的量之比1:2充入CO和H2,发生反应:CO(g)+2H2(g)?CH3OH(g).测得平衡时CO的转化率随温度及压强的变化如图1所示.p2、195℃时,n(H2)随时间的变化如表所示.
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
(2)你认为p1<p2;p2、195℃时,B点,v(正)<v(逆)(填“<”“>”或“=”).
(3)p2、195℃时,该反应的化学平衡常数为25.
Ⅱ.NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如图2:
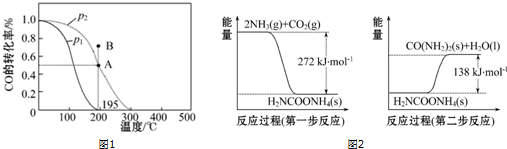
(1)NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-134kJ•mol-1.
(2)工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有D(填序号).
A.升高温度 B.加入催化剂
C.将尿素及时分离出去 D.增大反应体系的压强.
(1)某温度下,2SO2(g)+O 2(g)═2SO3(g)△H=-197kJ/mol.开始时在10L的密闭容器中加入8.0mol SO2(g)和20.0mol O 2(g),当反应达到平衡时共放出394kJ的热量,该温度下的平衡常数K=0.56(mol/L)-1(保留两位有效数字),若升高温度时,K将减小(填“增大、减小或不变”).
(2)若体积不变的条件下,下列措施中有利于提高SO2的转化率条件是AC(填字母).
A.通入氧气 B.移出氧气 C.增大压强 D.减小压强 E.加入催化剂
(3)根据下表提供的不同条件下SO2的转化率(%)的数据,试选择该反应的适宜条件(以V2O5作催化剂)温度450℃;压强1×105Pa.
| 压强 温度 | 1×105Pa | 5×105Pa | 10×105Pa | 50×105Pa | 100×105Pa |
| 450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 500℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO 3的浓度不变 D.c(SO 2)=c(SO 3)
E.v 正(SO 2)=v 正(SO 3) F.v 正(SO 3)=2v 逆(O 2)
Ⅱ研究化学反应原理对于生产生活是很有意义的.
(1)在0.10mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=2.2×10-8mol•L-1(Ksp[Cu(OH)2]=2.2×10-20).
(2)若在0.1mol•L-1硫酸铜溶液中通入H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是0.2mol•L-1.
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为吸热反应(填“吸热”、“放热”),写出该反应的平衡常数表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$.
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是bc.
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3)能判断该反应是否达到化学平衡状态的依据是bc.
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)若在(4)所处的温度下,在1L的密闭容器中,加入2molCO2和3molH2充分反应达平衡时,H2的物质的量为b,CO2的物质的量为c.
a.等于1.0mol b.大于1.0mol
c.大于0.5mol,小于1.0mol d.无法确定.
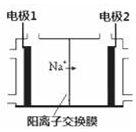 电解饱和食盐水是重要的化工产业,它被称为“氯碱工业”.在教材《化学1》、《化学2》、《化学反应原理》中均有提及,请写出电解饱和食盐水的化学反应方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.其中图2是《化学反应原理》中电解饱和食盐水工业中所采用的离子交换膜电解槽示意图,部分图标文字已被除去,请根据图中残留的信息,通电以后,Na+向右侧移动,可判断出电极2 是阴极,在该电极周围的溶液中,NaOH浓度将会变大(填“变大”或“减小”或“不变”);电极1上的电极反应式为2Cl--2e-=Cl2↑.
电解饱和食盐水是重要的化工产业,它被称为“氯碱工业”.在教材《化学1》、《化学2》、《化学反应原理》中均有提及,请写出电解饱和食盐水的化学反应方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.其中图2是《化学反应原理》中电解饱和食盐水工业中所采用的离子交换膜电解槽示意图,部分图标文字已被除去,请根据图中残留的信息,通电以后,Na+向右侧移动,可判断出电极2 是阴极,在该电极周围的溶液中,NaOH浓度将会变大(填“变大”或“减小”或“不变”);电极1上的电极反应式为2Cl--2e-=Cl2↑.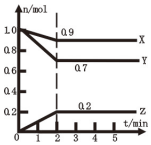 (1)某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.
(1)某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.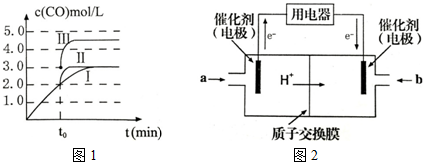
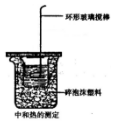 某同学用如图装置做中和热的测定实验
某同学用如图装置做中和热的测定实验