题目内容
 50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
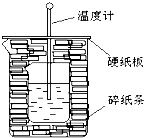
50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,有两处缺点,其一是
(2)烧杯间填满碎纸条的作用是
(3)若大烧杯上不盖硬纸板,求得的反应热数值
(4)实验中该用60mL0.50mol?L-1盐酸跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
(6)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为①2.2℃②2.4℃③3.4℃,则最终代入计算式的温差均值为
考点:中和热的测定
专题:实验题
分析:(1)大小烧杯口不对齐,会使一部分热量散失;根据量热计的构造结合实验原理来判断该装置的错误;
(2)中和热测定实验成败的关键是保温工作;
(3)操作时大烧杯上如不盖硬纸板,会使一部分热量散失
(4)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(5)氨水为弱碱,电离过程为吸热过程;
(6)先判断温度差的有效性,然后求出温度差平均值.
(2)中和热测定实验成败的关键是保温工作;
(3)操作时大烧杯上如不盖硬纸板,会使一部分热量散失
(4)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(5)氨水为弱碱,电离过程为吸热过程;
(6)先判断温度差的有效性,然后求出温度差平均值.
解答:
解:(1)大小烧杯口不对齐,会使一部分热量散失;由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:两烧杯口没有对齐;没有环形玻璃搅棒器;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)若大烧杯上不盖硬纸板,会使一部分热量散失,求得的反应热数值偏小,故答案为:偏小;
(4)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,测得中和热数值相等,
故答案为:不相等;相等;
(5)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于中和热数值;故答案为:偏小;
(6)三次温度差分别为①2.2℃②2.4℃③3.4℃,第③组数据舍去,温度差平均值=
=2.3℃,故答案为:2.3.
故答案为:两烧杯口没有对齐;没有环形玻璃搅棒器;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)若大烧杯上不盖硬纸板,会使一部分热量散失,求得的反应热数值偏小,故答案为:偏小;
(4)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,测得中和热数值相等,
故答案为:不相等;相等;
(5)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于中和热数值;故答案为:偏小;
(6)三次温度差分别为①2.2℃②2.4℃③3.4℃,第③组数据舍去,温度差平均值=
| 2.2℃+2.4℃ |
| 2 |
点评:本题综合考查了中和热的测定、误差分析,可以根据所学知识进行回答,难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
旅游洞穴一般是指供游人观览的喀斯特洞穴,多姿多彩的钟乳石,石笋,石柱,石花等碳酸钙沉积体是喀斯特洞穴中的主要景观.由于游人呼吸有时会使旅游洞穴中二氧化碳浓度大幅度升高,可能造成的后果是( )
①抑制碳酸钙沉积体的生长
②促进碳酸钙沉积体的生长
③使游客有憋闷的感觉
④使照明灯下的植物大量死亡.
①抑制碳酸钙沉积体的生长
②促进碳酸钙沉积体的生长
③使游客有憋闷的感觉
④使照明灯下的植物大量死亡.
| A、①③ | B、②③ | C、①④ | D、②④ |
下列离子检验的方法正确的是( )
| A、某待测液加入AgNO3溶液,生成白色沉淀,说明原溶液中有Cl- |
| B、某待测液加入BaCl2溶液,生成白色沉淀,说明原溶液中有SO42- |
| C、某待测液加入CaCl2溶液,生成白色沉淀,说明原溶液中有CO32- |
| D、某待测液加入NaOH溶液,生成蓝色沉淀,说明原溶液中有Cu2+ |
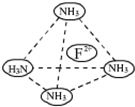 物质结构与性质A、B、C、D、E为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子2p原子轨道上有3个未成对的电子,且B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,F原子核外最外层只有1个电子,其余各层均充满电子.
物质结构与性质A、B、C、D、E为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子2p原子轨道上有3个未成对的电子,且B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,F原子核外最外层只有1个电子,其余各层均充满电子.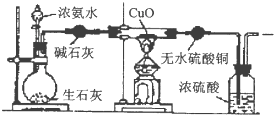
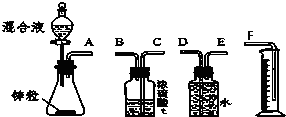 某学习小组在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.为了进一步研究硫酸铜的浓度对氢气生成速率的影响,该小组同学开始了实验探究.
某学习小组在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.为了进一步研究硫酸铜的浓度对氢气生成速率的影响,该小组同学开始了实验探究.