题目内容
17.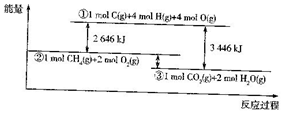 如图表示甲烷和氧气反应过程中的能量变化:请回答下列问题:
如图表示甲烷和氧气反应过程中的能量变化:请回答下列问题:(1)甲烷燃烧反应中,反应物的总能量大于,(填“大于”“小于或“等于”生成物的总能量.
(2)甲烷燃烧可能生成水蒸汽,也可能生成液态水.相同条件下,如果反应生成1molCO2(g)与2mot H2O(1),若将其标在图中,则其位置应在A(填代号).
A.③下方 B.②与③之间
C.①与②之间 D.①上方
(3)根据图中数据计算,1mol CH4 (g)和2mol O2(g)的总能量之差为800 kJ.若一定量的CH4与O2 发生上述反应时的能量变化为200kJ,则生成C=0键的物质的量为 0.5mol.
(4)已知破坏1mol C-H键需要吸收415kJ能量,则破坏1mol O=O中的化学键需要吸收的能量为493kJ.
分析 (1)所有的燃烧反应是放热反应,故反应物的总能量大于生成物的总能量;
(2)液态水所含的总能量低于气态水所含的总能量;
(3)总能量之差=生成物总能量-反应物总能量;1molCH4 参与反应放出800J的热量,当能量变化为200kJ时,则参与反应的CH4 0.25mol,据元素守恒,则生成0.25molCO2,CO2结构简式为O=C=O,故有0.5molO=C键;
(4)由图象可知破坏4mol C-H键和2molO-O键,所需要吸收2646kJ能量,其中破坏4mol C-H键需要吸收4×415kJ=1660kJ能量,所以破坏1mol氧气中的 O=O中的化学键需要吸收的能量为$\frac{1}{2}$(2646-1660)kJ=493kJ,据此分析.
解答 解:(1)所有的燃烧反应是放热反应,故反应物的总能量大于生成物的总能量,
故答案为:大于;
(2)液态水所含的总能量低于气态水所含的总能量,故在③的下方,
故答案为:A;
(3)总能量之差=生成物总能量-反应物总能量,故1mol CH4 (g)和2mol O2(g)的总能量之差为(3446-2646)=800KJ;1molCH4 参与反应放出800J的热量,当能量变化为200kJ时,则参与反应的CH4 0.25mol,据元素守恒,则生成0.25molCO2,CO2结构简式为O=C=O,故有0.5molO=C键,
故答案为:800;0.5;
(4)由图象可知破坏4mol C-H键和2molO-O键,所需要吸收2646kJ能量,其中破坏4mol C-H键需要吸收4×415kJ=1660kJ能量,所以破坏1mol氧气中的 O=O中的化学键需要吸收的能量为$\frac{1}{2}$(2646-1660)kJ=493kJ,
故答案为:493.
点评 本题考查了化学反应能量变化、依据化学键能计算反应能量变化,主要是基础的熟练掌握,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 1-丁烯的键线式: | B. | 乙烯的分子式:CH2=CH2 | ||
| C. | -CHO的电子式: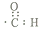 | D. | 丙烷分子的比例模型为: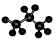 |
| A. | 葡萄糖制镜利用了葡萄糖的氧化性 | |
| B. | 室温下,在水中的溶解度:乙醇>苯酚>乙酸乙酯 | |
| C. | 酯在碱性条件下水解生成对应的酸和醇 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼 |
| A. | 同系物的化学性质一定相似 | |
| B. | 卤代烃在氢氧化钠醇溶液中共热均能发生消去反应 | |
| C. | 1mol醛与银氨溶液反应只能还原出2molAg | |
| D. | 在催化剂作用下,丙醛、丙酮、丙酸均能与氢气发生加成反应 |
| A. | 氢氟酸可蚀刻玻璃说明氢氟酸具有强酸性 | |
| B. | 油脂的氢化说明油脂分子中含有不饱和键 | |
| C. | 维生素C常用作抗氧化剂说明它具有氧化性 | |
| D. | 汽车尾气中含有氮氧化物说明汽油中含有氮元素 |
| A. | 食盐可作调味剂,也可以用作食品防腐剂 | |
| B. | 碳酸钾有一定的去污能力,在热水中去污能力会减弱 | |
| C. | 煤经过气化和液化等变化后,可以减少PM2.5引起的污染 | |
| D. | 根据纤维燃烧产生的气味,不能确定是否为蛋白质纤维 |
| A. | 22.4LNH3分子中含有3NA个N-H键 | |
| B. | 2.3 g Na完全与O2反应生成3.6 g产物时失去的电子数为0.1NA | |
| C. | 1 L0.1 mol•L-1蔗糖溶液中所含分子数为0.1NA | |
| D. | 常温常压下,46g NO2含有的原子数小于3NA |
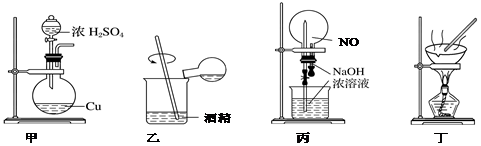
| A. | 用图甲做铜与浓硫酸反应制取SO2 | |
| B. | 用图乙配制浓硫酸与酒精的混合液 | |
| C. | 用图丙做NO与NaOH溶液的“喷泉”实验 | |
| D. | 用装置丁做蒸发CuCl2溶液获得CuCl2•2H2O |
| A. | 乙烷与氯气光照反应可以制得较纯净的1,2-二氯乙烷 | |
| B. | 苯中的化学键都是非极性键 | |
| C. | 煤的干馏属于物理变化 | |
| D. | 涤纶、酚醛树脂和蛋白质都属于高分子化合物 |