题目内容
2.已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4.则下列说法正确的是( )| A. | 气态氢化物的稳定性:HX<H2Y<ZH3 | |
| B. | 非金属活泼性:Y<X<Z | |
| C. | 原子半径:X>Y>Z | |
| D. | 原子最外电子层上电子数的关系:Y=$\frac{1}{2}$(X+Z) |
分析 X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4,元素的非金属性越强,其最高价氧化物的水化物酸性越强,所以元素非金属性X>Y>Z,
A.元素的非金属性越强,其气态氢化物的稳定性越强;
B.元素的非金属性越强,其非金属活泼性越强;
C.同一周期元素,元素非金属性越强,其原子半径越小;
D.根据最高价含氧酸HXO4、H2YO4、H3ZO4判断X、Y、Z的最外层电子数.
解答 解:X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4,元素的非金属性越强,其最高价氧化物的水化物酸性越强,则元素非金属性X>Y>Z,
A.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性X>Y>Z,所以气态氢化物的稳定性:HX>H2Y>ZH3,故A错误;
B.元素的非金属性越强,其非金属活泼性越强,所以其非金属活泼性X>Y>Z,故B错误;
C.同一周期元素,元素非金属性越强,其原子半径越小,所以原子半径X<Y<Z,故C错误;
D.根据最高价含氧酸HXO4、H2YO4、H3ZO4可知,X、Y、Z的最外层电子数分别为7、6、5,所以原子最外电子层上电子数的关系:Y=$\frac{1}{2}$(X+Z),故D正确;
故选D.
点评 本题考查位置、结构与性质关系的应用,题目难度不大律,明确元素周期律内容为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
14.某溶液能与铝片反应产生氢气,该溶液中一定不能大量共存的离子组是( )
| A. | Fe2+、Cl-、NO3-、K+ | B. | K+、Mg2+、Cl-、SO42- | ||
| C. | Na+、Br-、NO3-、S2- | D. | K+、CO32-、Na+、AlO2- |
10.下列各组物质中互为同位素的是( )
| A. | 136C和146C | B. | CH3CH2CH2CH3和CH3CH(CH3)CH3 | ||
| C. | 红磷和白磷 | D. | 甲烷和乙烷 |
7.实验室制取下列气体时,只能用排水法收集的是( )
| A. | CH4 | B. | SO2 | C. | NO | D. | NO2 |
14.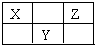 X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )
X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )
 X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )
X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )| A. | 原子序数由大到小为 Z>Y>X | |
| B. | 氢化物最稳定的元素为Z | |
| C. | 最高价氧化物的水化物酸性最强的元素为Z | |
| D. | 原子半径由大到小为 Y>Z>X |
11.下列现象与氢键有关的是( )
①HF的熔、沸点比HCl的熔、沸点高②NH3极易溶于水③冰的密度比液态水的密度小④水分子高温下很稳定.
①HF的熔、沸点比HCl的熔、沸点高②NH3极易溶于水③冰的密度比液态水的密度小④水分子高温下很稳定.
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ①③ |
12.下列变化属于物理变化的是( )
| A. | O2在放电条件下变成O3 | B. | 加热胆矾成无水硫酸铜 | ||
| C. | 漂白的草帽久置于空气中变黄 | D. | 石油分馏 |