题目内容
类推的思维方法在化学学习与研究中经常用到,但有时会产生错误的结论.因此,推出的结论最终要经过实践的检验才能决定其是否正确.以下几种类推结论中,正确的是( )
| A、第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| B、IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| C、Fe3O4可以写成FeO3;Pb3O4也可以写成PbO?Pb2O3 |
| D、NaHSO4与NaHSO3溶于水显酸性,由所有酸式盐溶于水显酸性 |
考点:元素周期律的作用,盐类水解的应用
专题:
分析:A、元素的非金属性越强,其气态氢化物的稳定性越大;
B、VA族中,N的非金属性最强,NH3中分子之间存在氢键,据此分析即可;
C、Pb在化合物里显+2价或+4价,根据化合价代数和为零的原则写出Pb的两种氧化物形式为:PbO和PbO2;
D、强酸的酸式盐溶于水呈酸性,比如:硫酸氢钠.
B、VA族中,N的非金属性最强,NH3中分子之间存在氢键,据此分析即可;
C、Pb在化合物里显+2价或+4价,根据化合价代数和为零的原则写出Pb的两种氧化物形式为:PbO和PbO2;
D、强酸的酸式盐溶于水呈酸性,比如:硫酸氢钠.
解答:
解:A、元素的非金属性越强,稳定性越大,同周期元素从左到右元素的非金属性逐渐增强,则对应的氢化物的稳定性逐渐增强,故A正确;
B、因第ⅤA族中,N的非金属性最强,且氨气中分子之间存在氢键,则氨气的熔、沸点比其他元素氢化物的高,故B错误;
C、Pb在化合物里显+2价或+4价,根据化合价代数和为零的原则写出Pb的两种氧化物形式为PbO和PbO2,那么Pb2O3的氧化物的表示形式可以写成PbO?PbO2,故C错误;
D、强酸的酸式盐溶于水呈酸性,比如:硫酸氢钠,故D错误,
故选A.
B、因第ⅤA族中,N的非金属性最强,且氨气中分子之间存在氢键,则氨气的熔、沸点比其他元素氢化物的高,故B错误;
C、Pb在化合物里显+2价或+4价,根据化合价代数和为零的原则写出Pb的两种氧化物形式为PbO和PbO2,那么Pb2O3的氧化物的表示形式可以写成PbO?PbO2,故C错误;
D、强酸的酸式盐溶于水呈酸性,比如:硫酸氢钠,故D错误,
故选A.
点评:本题考查元素周期表和元素周期律的应用,为高频考点,把握元素的位置、性质的变化规律为解答的关键,侧重金属性、非金属性比较的考查,题目难度不大.

练习册系列答案
相关题目
下列关于有机物的命名中不正确的是( )
| A、2,2─二甲基戊烷 |
| B、2─乙基戊烷 |
| C、3,4─二甲基辛烷 |
| D、3─甲基己烷 |
下列事实不能用勒夏特列原理解释的是( )
| A、由H2、I2(g)、HI组成的平衡体系加压后颜色变深 |
| B、黄绿色的氯水光照后颜色变浅 |
| C、使用催化剂可加快SO2转化为SO3的速率 |
| D、在含有Fe(SCN)2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
四种短周期元素的性质或结构信息如下表,下列推断错误的是( )
| 元素编号 | 元素性质或结构 |
| T | M层上有2对成对电子 |
| X | 元素最高正价是+7价 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | 单质是银白色固体、导电、密度比水小,与水剧烈反应、和氧气反应不同条件下产物不同 |
| A、T的氢化物是同周期元素氢化物中最不稳定的 |
| B、X的最高价氧化物对应的水化物,是无机含氧酸中的最强酸 |
| C、离子半径从小到大的顺序:Y<Z<T<X |
| D、X、T形成化合物的类型与X、Z形成化合物的类型不同 |
将质量分数为a%的NaOH溶液蒸发掉mg水后,变成VmL2a%的NaOH不饱和溶液,则蒸发后的溶液的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
等物质的量的下列物质分别跟盐酸反应,消耗HCl的物质的量最多的是( )
| A、Na2O2 |
| B、Na2CO3 |
| C、Al2O3 |
| D、Al(OH)3 |
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A、Na+结构示意图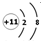 | ||||
B、质量数为16的氧原子:
| ||||
| C、纯碱的化学式:NaHCO3 | ||||
D、铁丝在氯气中燃烧的化学方程式:Fe+Cl2
|