题目内容
下列有关能量的判断或表示方法正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| B、从C(石墨)═C(金刚石)△H═+1.9kJ?mol-1,可知石墨比金刚石更稳定 |
| C、2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2 H2O(l)△H=-285.8 kJ?mol-1 |
| D、由H+(aq)+OH-(aq)═H2O(l)△H═-57.3 kJ?mol-1,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.3 kJ |
考点:反应热和焓变,热化学方程式
专题:化学反应中的能量变化
分析:A、等质量的硫蒸气比硫固体的能量高;
B、石墨变金刚石吸热,所以石墨比金刚石更稳定;
C、氢气的燃烧热应用1mol表示;
D、起始强碱稀溶液完全燃烧生成1mol水放出的热量为中和热,CH3COOH为弱酸放出热量小于57.3 kJ.
B、石墨变金刚石吸热,所以石墨比金刚石更稳定;
C、氢气的燃烧热应用1mol表示;
D、起始强碱稀溶液完全燃烧生成1mol水放出的热量为中和热,CH3COOH为弱酸放出热量小于57.3 kJ.
解答:
解:A、等质量的硫蒸气比硫固体的能量高,燃烧生成二氧化硫气体,前者放出热量更多,故A错误;
B、能量越高越活泼,石墨变金刚石吸热,所以石墨比金刚石更稳定,故B正确;
C、氢气的燃烧热应用1mol表示,氢气燃烧的热化学方程式为:H2(g)+
O2(g)═H2O(l)△H=-285.8 kJ?mol-1,故C错误;
D、CH3COOH为弱酸放出热量小于57.3 kJ,故D错误;
故选B.
B、能量越高越活泼,石墨变金刚石吸热,所以石墨比金刚石更稳定,故B正确;
C、氢气的燃烧热应用1mol表示,氢气燃烧的热化学方程式为:H2(g)+
| 1 |
| 2 |
D、CH3COOH为弱酸放出热量小于57.3 kJ,故D错误;
故选B.
点评:本题考查了反应能量和分析,燃烧热、中和热概念理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
俄罗斯科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果成功制成4个第115号元素的原子,其与N元素同主族.这4个原子在生成数微秒后衰变成第113号元素.前者的一种核素为
X.下列有关叙述正确的是( )
288 115 |
| A、115号元素衰变成113号元素是化学变化 | ||
B、核素
| ||
| C、113号元素其质量数为113 | ||
| D、因115号元素与N元素同主族,所以定为非金属元素 |
某无色透明溶液,在酸性环境下能大量共存的离子组是( )
| A、Na+K+AlO2-Cl- |
| B、Na+SO42-HCO3-C1- |
| C、K+MnO4- NO3-Fe2+ |
| D、Mg2+Cl-NH4+SO42- |
下列叙述正确的是( )
| A、1摩尔氧 |
| B、有大量有毒易燃气体在室内扩散,不能立即打开排风扇开关 |
| C、1L水中溶解224 L HCl气体(标准状况下测得)后形成溶液物质的量浓度为10 mol?L-1 |
| D、将7.4克氢氧化钙放入烧杯中,加水搅拌冷却后全部转移到100 mL容量瓶并加水至刻度线,浓度为1 mol?L-1 |
下列操作或叙述正确的是( )
| A、配制1mol?L-1NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶 | ||
| B、用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶 | ||
C、向某溶液中加入BaCl2溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有S
| ||
| D、向沸水中逐滴滴加1mol?L-1FeCl3溶液,并不断用玻璃棒搅拌,可制得Fe(OH)3胶体 |
大气层中的臭氧层(O3)能吸收太阳光中的紫外线,下列关于O3的分类正确的是( )
| A、化合物 | B、单质 |
| C、氧化物 | D、混合物 |
以下有关原予结构及元素周期律的叙述正确的是( )
| A、同主族元素从上到下,单质的熔点逐渐降低 |
| B、同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C、第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D、第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
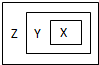 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )