题目内容
(9分)向30.0mL硫酸铜溶液中加入过量铝粉,待充分反应后,再向其中加入2.00mol/L烧碱溶液,至沉淀不再减少,消耗烧碱溶液210mL,且收集到气体0.672L(标准状况)。据此计算:
(1)加入铝粉的质量。
(2)原硫酸铜溶液的物质的量浓度。
(1)3.24克 (2) 5mol/L
【解析】
试题分析:产生气体0.672L物质的量为:n=0.672L÷22.4/Lmol=0.03mol,设生成0.03molH2消耗的铝和NaOH的物质的量为n1和 n2,则有:
2 Al + 2 NaOH + 2H2O = 2Na Al O + 3 H2↑
2 2 3
n1 n2 0.03mol 得: n1 = n2 = 0.02mol
Al3+与消耗的NaOH的物质的量为:0.21L×2.00mol/L-0.02mol=0.40mol,设Al3+物质的量为Al3+,有:
Al3+ + 4OH- = AlO2- + 2H2O
1 4
n3 0.40mol, n3=0.1mol,n(Al)= n1+ n3= 0.02mol+0.1mol=0.12 mol,铝粉的质量为:m=0.12mol×27g/mol=3.24g
设硫酸铜的物质的量为n4,则:
3Cu2+ + 2 Al=3Cu + 2Al3+
3 2
n4, 0.1mol
得:n4=0.15mol,c(CuSO4)=0.15mol÷0.03L=5mol/L
考点:离子方程式的书写和物质的量的计算。

仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图1、图2)就能实现相应实验目的是
选项 | A | B | C | D |
实验项目 | 除去KCl中少 的 MnO2 | 用10mol/L的盐酸配制100mL0.1mol/L的盐酸 | 用氯化钠溶液制备氯化钠晶体 | 除去CO2气体中的HCl |
实验仪器 或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 |
图1 |
图2 |





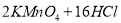 (浓)====
(浓)==== 

 溶液吸收氯气防止污染。写出该反应的离子方程式 。
溶液吸收氯气防止污染。写出该反应的离子方程式 。