题目内容
16.下列物质中,能与镁反应并生成氢气的是( )| A. | 碳酸钠溶液 | B. | 苯酚 | C. | 醋酸溶液 | D. | 二氧化碳 |
分析 金属镁的金属强较强,可以和酸或是水解显酸性的盐溶液反应生成氢气,以此解答该题.
解答 解:A.碳酸钠溶液中碳酸根离子水解显碱性,不能和金属镁反应,故A错误;
B.常温下镁和苯酚不反应,在加热条件下,镁与苯酚反应可生成氢气,故B正确;
C.CH3COOH属于羧酸,具有酸的通性,其溶液可以和金属镁反应产生氢气,故C正确;
D.Mg能在二氧化碳中燃烧生成MgO与碳,不可能反应生成氢气,故D错误.
故选BC.
点评 本题考查学生金属镁的化学性质,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
6.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 常温下0.1 mol•L-1的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,c(NH4+)由大到小的顺序为②>①>③ | |
| B. | 常温下0.4 mol•L-1CH3COOH溶液和0.2 mol•L-1 NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.2 mol•L-1 NaHCO3溶液等体积混合所得溶液中:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) | |
| D. | 0.1 mol•L-1的氨水与0.05 mol•L-1 H2C2O4溶液等体积混合所得溶液中:c(NH4+)+c(NH3•H2O)=2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4) |
7.设NA是阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| B. | 42克由C2H4和C5H10组成的混合气体中含共用电子对数目为9NA个 | |
| C. | 25℃时,50 g 98%浓硫酸和50 g 98%浓磷酸混合后含氧原子数为4NA | |
| D. | 12 g石墨烯(单层石墨)中含有六元环的个数为NA |
4.下列有关物质变化的说法正确的是( )
| A. | 熔融态的Al2O3导电、12C转化为14C都属于化学变化 | |
| B. | 根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类 | |
| C. | 用热的纯碱溶液洗涤沾有油污的器具时涉及化学变化和物理变化 | |
| D. | 将盛有NO2气体的密封烧瓶,放入热水中气体颜色加深的变化是物理变化 |
11.1mol的V2O5与足量铝反应,转移电子的物质的量是( )
| A. | 4mol | B. | 6mol | C. | 8mol | D. | 10mol |
1.如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断不正确的是( )
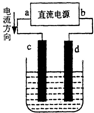

| A. | a为正极 | |
| B. | c极上发生氧化反应 | |
| C. | 电解过程中铜离子移向d极 | |
| D. | 电解过程中,d的电极反应式为:2Cl--2e-=Cl2↑ |
8.在主族元素X、Y、Z中,X与Y两元素的原子核外电子层数相同;X的原子半径大于Y的原子半径,X与Z两原子的阳离子具有相同的电子结构,Z的离子半径大于X的离子半径,则X、Y、Z三种元素的原子序数最大的是( )
| A. | X | B. | Y | C. | Z | D. | 无法确定 |
12.根据下列反应事实:①X+Y2+=X2++Y;②Z+2H2O(冷)=Z(OH)2+H2↑;③Z2+氧化性比X2+弱;④由Y、W电极组成的电池,Y电极反应为Y-2e-=Y2+,可知X、Y、Z、W的还原性强弱顺序为( )
| A. | X>Z>Y>W | B. | Z>X>Y>W | C. | Z>Y>X>W | D. | Z>W>X>Y |