题目内容
10.设NA表示阿伏加德罗常数的值.下列说法正确的是( )| A. | 标准状况下,7.8g Na2O2中含有的阴离子的数目为0.2NA | |
| B. | 1mol/L的CaCl2溶液中含有的Cl-为2NA | |
| C. | 1mol金属钠与足量氧气反应生成Na2O或Na2O2时,失去的电子数目均为NA | |
| D. | 常温常压下,18g水中含有的水分子数目为NA |
分析 A.Na2O2的摩尔质量为78g/mol;
B.没有告诉CaCl2溶液的体积,无法计算溶液中钠离子数目;
C.1mol钠完全反应失电子1mol;
D.质量转化为物质的量.
解答 解:A.Na2O2的摩尔质量均为78g/mol,故7.8g过氧化钠的物质的量为0.1mol,故0.1mol过氧化钠中含0.1mol阴离子即0.1NA个,故A错误;
B.没有告诉CaCl2溶液的体积,无法计算溶液中溶质的物质的量及氯离子数目,故B错误;
C.1mol钠完全反应失电子1mol,生成Na2O和Na2O2的混合物,转移电子总数NA,故C正确;
D.常温常压下,18 g水中含有的水分子数目:$\frac{18g}{18g/mol}$×NA=NA,故D正确.
故选CD.
点评 本题考查了阿伏伽德罗常数的应用,把握以物质的量为中心的有关计算公式是解题关键,题目难度不大.

练习册系列答案
相关题目
20.无色溶液中可以大量共存的是( )
| A. | Fe3+ Cl -Na+SO42- | B. | MnO4-K+Cl-Na+ | ||
| C. | NH4+SO42-OH-Na+ | D. | CO32- HCO3- K+ Na+ |
18.下列说法正确的是( )
| A. | 用石墨电极电解FeCl3溶液,阴极反应:2Fe3++6H2O+6e-=2Fe(OH)3↓+3H2↑ | |
| B. | 1 mol•L-1的NH4Cl溶液中含有NH4+的数目一定小于NA | |
| C. | NaHCO3溶液加水稀释,$\frac{c(N{a}^{+})}{c(HC{{O}_{3}}^{-})}$的比值保持增大 | |
| D. | 将带有相反电荷的胶体混合,一定会出现胶体聚沉现象 |
5.环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动过度排放有关物质引起的.下列环境问题与所对应的物质不相关的是( )
| A. | 温室效应--二氧化硫 | B. | 光化学污染--二氧化氮 | ||
| C. | 酸雨--二氧化硫 | D. | 臭氧层破坏--氟氯烃 |
15.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Na+、K+、ClO-、Cl- | B. | Mg2+、Na+、SO42-、Cl- | ||
| C. | Ca2+、HCO3-、NO3-、K+ | D. | Na+、Cu2+、SO42-、NO3- |
2.关于下列各实验装置的叙述中,正确的是( )
| A. | 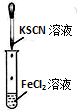 装置溶液变红色 | |
| B. | 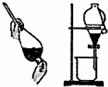 装置可用于分离乙醇和水的混合物 | |
| C. | 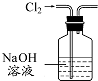 装置可除去Cl2中含有的少量HCl气体 | |
| D. | 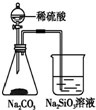 装置所示实验可验证酸性:H2SO4>H2CO3>H2SiO3 |
19.下列属于电解质的是( )
| A. | 酒精 | B. | 稀盐酸 | C. | 铜 | D. | 烧碱 |
20.下列说法正确的是( )
| A. | 秸秆、毛发及塑料完全燃烧都只生成二氧化碳和水 | |
| B. | 纤维素、油脂、蛋白质都能发生水解反应,都属于天然有机高分子化合物 | |
| C. | 苯和乙烯都能使溴水褪色,均与溴发生加成反应 | |
| D. | 蛋白质遇饱和硫酸铵溶液产生的沉淀能重新溶于水 |
 ;
;