题目内容
已知在0.1mol/L的CH3COOH溶液中,CH3COOH的电离常数Ka=1.8×10-5,则pH= .
考点:pH的简单计算
专题:
分析:根据醋酸的电离平衡常数等于醋酸根离子浓度和氢离子浓度乘与醋酸浓度的比值来计算.
解答:
解:0.1mol/L的CH3COOH溶液中,CH3COOH的电离常数Ka=
=1.8×10-5,醋酸根离子和氢离子浓度相等,所以c(H+)=
=1.35×10-3mol/L,所以pH≈3,故答案为:3.
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
| 1.8×10-5×0.1 |
点评:本题考查学生醋酸的电离平衡常数以及pH有关计算知识,难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,2.24L苯中含0.6NA个氢原子 |
| B、22.4LCl2通入水中充分反应,共转移NA个电子 |
| C、1L1mol?L-1氯化铜溶液中Cu2+的数目小于NA |
| D、0.1mol铁在0.1molCl2中充分燃烧,转移的电子数为0.3NA |
根据表提供的数据,下列判断正确的是( )
| 化学式 | 电离常数 |
| HF | Ka=3.5×10-4 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| HClO | Ka=3.2×10-8 |
| A、同温同浓度下,溶液的pH值:NaF>NaClO>Na2CO3 |
| B、结合H+ 的能力:ClO->CO32->F- |
| C、碳酸钠溶液中加入少量氢氟酸的离子方程式:CO32-+2HF=2F-+H2O+CO2↑ |
| D、次氯酸钠溶液中通少量二氧化碳的离子方程式:ClO-+CO2+H2O=HCO3-+HClO |
235 92 |
235 92 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
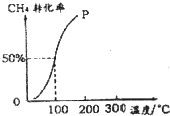 甲醇可作为燃料电池的原料.以CH4和H2O为原料,通过下列反应来制备甲醇.
甲醇可作为燃料电池的原料.以CH4和H2O为原料,通过下列反应来制备甲醇.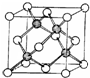 A、B、C、D、E五种元素的原子序数依次增大,其中A为周期表中原子半径最小的元素;B原子的最外层电子数是其次外层电子数的2倍;C是地壳中含量最高的元素;Cn-与D+具有相同的电子层结构; E原子的3d能级中成对电子数与未成对电子数之比为4:3.试回答下列问题:
A、B、C、D、E五种元素的原子序数依次增大,其中A为周期表中原子半径最小的元素;B原子的最外层电子数是其次外层电子数的2倍;C是地壳中含量最高的元素;Cn-与D+具有相同的电子层结构; E原子的3d能级中成对电子数与未成对电子数之比为4:3.试回答下列问题: