题目内容
8.下列关于浓硝酸和浓硫酸的叙述正确的是( )| A. | 露置在空气中,容器内酸液的质量都减轻 | |
| B. | 常温下都能与铜较快反应 | |
| C. | 常温下都能与氨气反应 | |
| D. | 加热条件下都能与碳反应 |
分析 A.浓硫酸具有吸水性、浓硝酸具有挥发性;
B.加热条件下,铜和浓硫酸能发生氧化还原反应;
C.常温下,氨气与硫酸反应生成硫酸铵,氨气与硝酸反应生成硝酸铵;
D.加热条件下,二者都能与碳发生氧化还原反应;
解答 解:A.浓硫酸具有吸水性,能吸收空气中的水蒸气,质量增加,浓硝酸具有挥发性,质量减轻,故A错误;
B.加热条件下,铜和浓硫酸发生氧化还原反应生成二氧化硫,常温下,铜和浓硝酸反应生成二氧化氮,故B错误;
C.常温下,氨气与硫酸反应生成硫酸铵,氨气与硝酸反应生成硝酸铵,所以两者都反应,故C正确;
D.加热条件下,浓硫酸和浓硝酸都与碳发生氧化还原反应生成气体氧化物和水,故D正确;
故选CD.
点评 本题考查了浓硫酸、浓硝酸的性质,根据浓硫酸和浓硝酸的强氧化性、与铁的钝化等知识点来分析解答即可,比较容易.

练习册系列答案
相关题目
4.钠、镁、铁、铜、硅、硫等元素中不能实现下列物质间直接转化有几种( )
单质→氧化物→酸或碱→盐.
单质→氧化物→酸或碱→盐.
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
19.在Al3++3H2O?Al(OH)3+3H+的平衡体系中,要使平衡向水解方向移动.且使溶液的pH增大,应采取的措施是( )
| A. | 加热 | B. | 通入HCl | ||
| C. | 加入适量的NaOH(固体) | D. | 加入固体NaCl |
3.一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2H2(g)+CO(g)?CH3OH(g)达到平衡,已知Ⅰ中的反应经过40min后达到平衡,则下列说法正确的是( )
| 容器 | 温度/k | 物质的起始浓度/mol•L-1 | CH3OH的平衡浓度/mol•L-1 | ||
| c(H2) | c(CO) | c(CH3OH) | |||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | Ⅰ中反应在0-40min内的平均速率为v(H2)=0.0020mol•L-1•min-1 | |
| B. | 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大 | |
| C. | 三个溶液中反应的平衡常数关系为Ⅱ=Ⅰ>Ⅲ | |
| D. | 若起始时向容器Ⅰ中充入0.020molH2、0.010molCO和0.010molCH3OH,则反应处于平衡状态 |
20.下列有关实验设计或操作正确且能达到目的是( )
| 选项 | A | B | C | D |
| 实验装置或操作 |  | 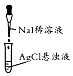 | 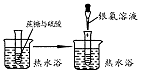 | 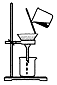 |
| 实验目的 | 配制一定物质的量浓度的稀硫酸 | 悬浊液由白色转为黄色证明Ksp(AgCl)大于Ksp(AgI) | 验证蔗糖在硫酸催化作用下发生水解反应 | 从碳酸氢钠悬浊液中分离出NaHCO3的晶体 |
| A. | A | B. | B | C. | C | D. | D |
18.设NA代表阿伏加德罗常数的数值,下列说法屮正确的是( )
| A. | 标准况状下,44.8 L四氯筑化碳含有的分子数为2NA | |
| B. | 0.1mol/L氯化铝溶液中含有Al3+数为0.1 NA | |
| C. | 1.8 g重水(D2O)中含有的质子数和电子数均为NA | |
| D. | 常温下,O2和O3的混合气体共16g中含有的氧原子数为NA |
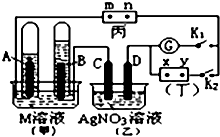 如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1,回答下列问题:
如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1,回答下列问题: