题目内容
四种易溶于水的强电解质A、B、C、D由以下7种离子组成(电解质中阴离子各不相同).
已知:①A、C溶液显碱性,A、B的溶液中水的电离程度相同;②C和D的溶液混合反应的现象只是有白色沉淀生成,B和C的溶液混合反应的现象只是有刺激性气味的气体生成,A和D的溶液混合无明显现象.
(1)A是 ,B是 .
(2)写出C与D的溶液反应的离子方程式 .
(3)将等体积、等物质的量浓度的B溶液和C溶液混合反应后溶液中各种离子浓度由大到小的顺序是 .
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
(1)A是
(2)写出C与D的溶液反应的离子方程式
(3)将等体积、等物质的量浓度的B溶液和C溶液混合反应后溶液中各种离子浓度由大到小的顺序是
考点:几组未知物的检验,常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:①A、C溶液的pH均大于7,应为醋酸盐和碱溶液,A、B的溶液中水的电离程度相同,则溶液水解程度相同;
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象,则说明C为Ba(OH)2,D为Na2SO4,则B为NH4Cl,A为CH3COONa,以此解答该题.
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象,则说明C为Ba(OH)2,D为Na2SO4,则B为NH4Cl,A为CH3COONa,以此解答该题.
解答:
解:①A、C溶液的pH均大于7,应为醋酸盐和碱溶液,A、B的溶液中水的电离程度相同,则溶液水解程度相同;
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象,则说明C为Ba(OH)2,D为Na2SO4,则B为NH4Cl,A为CH3COONa,
(1)根据题中信息推断出各物质分别为:A为CH3COONa,B为NH4Cl,C为Ba(OH)2,D为Na2SO4,
故答案为:CH3COONa;NH4Cl;
(2)C与D的溶液反应是Ba(OH)2和Na2SO4反应生成硫酸钡沉淀的过程,反应的离子方程式为:Ba2++SO42-=BaSO4↓;故答案为:Ba2++SO42-=BaSO4↓;
(3)等体积、等物质的量浓度的NH4Cl和Ba(OH)2混合反应后溶液中溶质是BaCl2、Ba(OH)2、NH3?H2O,则c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+);故答案为:c(OH-)> c(Ba2+)= c(Cl-)> c(NH4+)> c(H+).
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象,则说明C为Ba(OH)2,D为Na2SO4,则B为NH4Cl,A为CH3COONa,
(1)根据题中信息推断出各物质分别为:A为CH3COONa,B为NH4Cl,C为Ba(OH)2,D为Na2SO4,
故答案为:CH3COONa;NH4Cl;
(2)C与D的溶液反应是Ba(OH)2和Na2SO4反应生成硫酸钡沉淀的过程,反应的离子方程式为:Ba2++SO42-=BaSO4↓;故答案为:Ba2++SO42-=BaSO4↓;
(3)等体积、等物质的量浓度的NH4Cl和Ba(OH)2混合反应后溶液中溶质是BaCl2、Ba(OH)2、NH3?H2O,则c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+);故答案为:c(OH-)> c(Ba2+)= c(Cl-)> c(NH4+)> c(H+).
点评:本题较为综合,涉及无机物的推断、电解质在水溶液中的电离、盐类水解的应用等知识,难度较大,正确推断各种物质为解答本题的关键.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
将胆矾与生石灰、水按质量比为1:0.56:100混合配成无机铜杀菌剂波尔多液,其成分的化学式可表示为CuSO4?xCaSO4?xCu(OH)2?yCa(OH)2,当x=3时,y为( )
| A、1 | B、3 | C、5 | D、7 |
由Na2O2、Na2CO3、NaHCO3、NaCl固体中的某几种组成的混合物,向混合物中加入足量的盐酸,有气体放出,将放出的气体通入足量的NaOH溶液后,气体体积有所减少,若将上述混合物在空气中充分加热,也有气体放出,下列判断正确的是( )
| A、混合物中一定含有Na2O2、NaHCO3 |
| B、混合物中一定不含有Na2CO3和NaCl |
| C、混合物一定不含有Na2O2和NaCl |
| D、混合物中一定含有Na2O2、Na2CO3、NaHCO3 |
在0.1mol?L-1氨水中加入少量的NH4Cl晶体,则溶液的pH( )
| A、变大 | B、变小 |
| C、不变 | D、无法确定 |
下表列出了某短周期元素R的各级电离能数据(用I1、I2…表示,单位为kJ?mol-1).
下列关于元素R的判断中一定正确的是( )
| I1 | I2 | I3 | I4 | … | |
| R | 740 | 1 500 | 7 700 | 10 500 | … |
| A、R的最高正价为+3价 |
| B、R元素位于元素周期表中第ⅡA族 |
| C、R元素的原子最外层共有4个电子 |
| D、R元素基态原子的电子排布式为1s22s22p1 |
下列氧化物中,不会产生酸雨的是( )
| A、CO2 |
| B、NO |
| C、NO2 |
| D、SO2 |
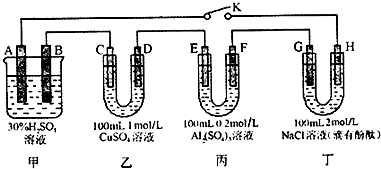
下列电池工作时能量转化形式与其它三个不同的是( )
 |  |  |  |
| A.锌锰碱性电池 | B硅太阳能电池 | C氢燃料电池 | D铅蓄电池 |
| A、A | B、B | C、C | D、D |
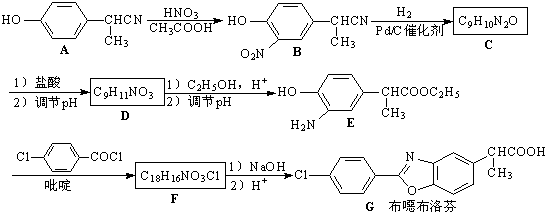

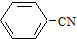 为原料制备
为原料制备 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH2=CH2
的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH2=CH2