题目内容
下列离子方程式不正确的是( )
| A、向Ba(OH)2溶液中滴加NH4HSO4溶液刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
| B、向Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、在NaOH溶液中通入少量的SO2气体:SO2+OH-=HSO3- |
| D、二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.沉淀刚好完全,氢氧化钡与硫酸氢铵按照物质的量1:1反应,硫酸氢铵中的铵根离子和氢离子恰好反应;
B.氢氧化钙少量,离子方程式按照氢氧化钙的组成书写,生成的碳酸根离子完全转化成碳酸钙沉淀;
C.二氧化硫少量,反应生成亚硫酸钠和水,不是生成亚硫酸氢根离子;
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,根据电荷守恒、质量守恒判断.
B.氢氧化钙少量,离子方程式按照氢氧化钙的组成书写,生成的碳酸根离子完全转化成碳酸钙沉淀;
C.二氧化硫少量,反应生成亚硫酸钠和水,不是生成亚硫酸氢根离子;
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,根据电荷守恒、质量守恒判断.
解答:
解:A.向Ba(OH)2溶液中滴加NH4HSO4溶液刚好沉淀完全,反应生成硫酸钡、一水合氨和水,反应的离子方程式为:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O,故A正确;
B.向Ca(HCO3)2溶液中加入少量Ca(OH)2溶液,反应生成碳酸钙沉淀和水,反应的离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H2O,故B正确;
C.在NaOH溶液中通入少量的SO2气体,反应生成亚硫酸钠和水,正确的 离子方程式为:SO2+2OH-=SO32-+H2O,故C错误;
D.二氧化硅与氢氧化钠溶液生成硅酸钠和水,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O,故D正确;
故选C.
B.向Ca(HCO3)2溶液中加入少量Ca(OH)2溶液,反应生成碳酸钙沉淀和水,反应的离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H2O,故B正确;
C.在NaOH溶液中通入少量的SO2气体,反应生成亚硫酸钠和水,正确的 离子方程式为:SO2+2OH-=SO32-+H2O,故C错误;
D.二氧化硅与氢氧化钠溶液生成硅酸钠和水,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O,故D正确;
故选C.
点评:本题考查了离子方程式的正误判断,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式,选项C为易错点,注意二氧化硫不足,反应生成亚硫酸钠.

练习册系列答案
相关题目
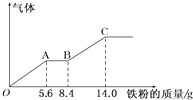 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果正确的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果正确的是( )| A、原混合酸中HNO3的物质的量为0.1 mol |
| B、OA段产生的是氢气,BC段产生NO |
| C、AB段的反应为Fe+2Fe(NO3)3═3 Fe(NO3)2 |
| D、H2SO4浓度为2.5 mol?L-1 |
现有几种物质①Al ②Al2O3 ③Al(OH)3 ④NaHCO3 ⑤NH4HCO3,其中既能跟盐酸反应,又能跟NaOH反应,而且均有气体放出的是( )
| A、①②③ | B、①④⑤ |
| C、①⑤ | D、④⑤ |
下列实验方法能达到目的是( )
| A、用氨水清洗试管内壁附着的银镜 |
| B、用饱和Na2CO3溶液除去乙醇中少量的乙酸和水 |
| C、制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| D、可用K3[Fe(CN)6]溶液鉴定FeCl3溶液中是否存在Fe2+ |
用NA表示阿伏加德罗常数,下列说法正确的是( )
A、2.9g C2H
| ||
| B、标准状况下,22.4L乙酸的分子数为NA个 | ||
| C、一个氯原子的质量是35.5NAg | ||
| D、铝与氢氧化钠溶液反应,每生成1mol氢气,铝就失去2NA个电子 |
已知下列热化学方程式:则14g CO气体还原足量FeO固体得到Fe单质和CO2气体时对应的△H约为( )
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
Fe2O3(s)+
CO(g)═
Fe3O4(s)+
CO2(g)△H=-15.73kJ/mol
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol.
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
Fe2O3(s)+
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol.
| A、-218 kJ/mol |
| B、-109 kJ/mol |
| C、+218 kJ/mol |
| D、+109 kJ/mol |
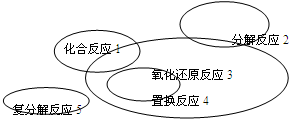
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于3区域的是 (3区域为除去1、2、4交叉部分)( )

| A、Cl2+2KBr═Br2+2KCl | ||||
B、CaCO3
| ||||
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
D、2CuO+2CO
|
 在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.