题目内容
6.对下列各溶液中,微粒的物质的量浓度关系表述正确的是( )| A. | CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO_)+c(CH3COOH)+2 c(Cl_) | |
| B. | 将pH=3的盐酸溶液和pH=11的氨水等体积混合后:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| C. | NaHCO3溶液中:c(OH-)=c(H+)+c(H2CO3)-c(CO32-) | |
| D. | 在25℃100 mL NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3•H2O)+c(OH-) |
分析 A.CH3COONa和CaCl2混合溶液中溶质存在物料守恒,c(Na+)=c(CH3COO-)+c(CH3COOH),2c(Ca2+)=c(Cl-);
B.将pH=3的盐酸溶液和pH=11的氨水等体积混合后一水合氨是弱电解质,又电离出铵根离子和氢氧根离子,溶液显碱性;
C.碳酸氢钠溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-),物料守恒c(Na+)=c(H2CO3)-c(CO32-)+c(HCO3-),据此计算判断;
D.在25℃100 mL NH4Cl溶液中存在物料守恒n(Cl)=n(N);
解答 解:A.CH3COONa和CaCl2混合溶液中溶质存在物料守恒,c(Na+)=c(CH3COO-)+c(CH3COOH),2c(Ca2+)=c(Cl-),CH3COONa和CaCl2混合溶液中CH3COONa和CaCl2混合溶液中醋酸钠和氯化钙的量不知,不能合并物料守恒,故A错误;
B.将pH=3的盐酸溶液和pH=11的氨水等体积混合后一水合氨是弱电解质,又电离出铵根离子和氢氧根离子,溶液显碱性,c(NH4+)>c(Cl-)>c(OH-)>c(H+)故B错误;
C.碳酸氢钠溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-),物料守恒c(Na+)=c(H2CO3)-c(CO32-)+c(HCO3-),据此计算判断c(OH-)=c(H+)+c(H2CO3)-c(CO32-),故C正确;
D.在25℃100 mL NH4Cl溶液中存在物料守恒c(Cl-)=c(NH4+)+c(NH3•H2O),故D错误;
故选C.
点评 本题考查了电解质溶液中盐类水解、弱电解质电离平衡、电解质溶液中电荷守恒、物料守恒分析判断,掌握基础是解题关键,题目难度中等.

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案| A. | pH试纸 | B. | 酚酞试液 | C. | 稀硫酸 | D. | 氯化钡溶液 |
| A. | HClO4、H3PO4、H2SO4的酸性依次减弱 | |
| B. | HCl、HBr、HI的稳定性依次减弱 | |
| C. | N、O、F原子半径逐渐增大 | |
| D. | 钠、镁、铝的还原性依次减弱 |
| A. | $\frac{4}{5}$v(NH3)=v(O2) | B. | 5v(O2)=6v(H2O) | C. | $\frac{2}{3}$v(NH3)=v(H2O) | D. | 4v(O2)=5v(NO) |
①Na2CO3②CH3COONa ③CH3CH2ONa ④NH4NO3⑤NaHSO4⑥苯酚钠 ⑦NaHCO3.
| A. | ③①⑥⑦②④⑤ | B. | ⑥①②⑦③④⑤ | C. | ⑤④③①⑥⑦② | D. | ⑥③⑦①②④⑤ |
| A. | 属于第二周期第VIA族元素 | B. | 原子最外层电子数为8 | ||
| C. | 质子数为16 | D. | 与167N互为同位素 |
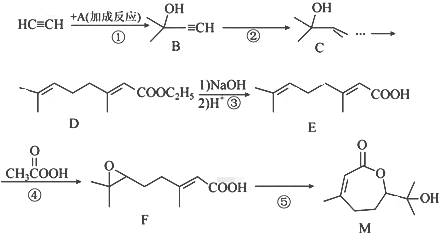
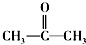 ,两分子HC≡CH与一分子A反应的产物的结构简式为
,两分子HC≡CH与一分子A反应的产物的结构简式为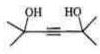 .
. .
. .
.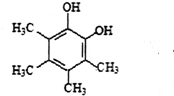 .
.