题目内容
某同学用下图所示装置制备并检验Cl2的性质。下列说法正确的是 ( )

A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B.Ⅱ图中:充分光照后,量筒中剩余气体约10 mL(条件相同)
C.Ⅲ图中:生成蓝色的烟,若在集气瓶中加入少量水,溶液呈绿色
D.Ⅳ图中:干燥的有色布条不褪色,湿润的有色布条能褪色,说明Cl2有漂白性
B
【解析】
试题分析:二氧化锰和浓盐酸在加热条件下反应生成氯气,但稀盐酸与二氧化锰不反应,当盐酸浓度降低时,反应停止,则盐酸不能完全消耗,故A错误;Ⅱ中涉及反应有Cl2+H2O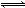 HCl+HClO,2HClO
HCl+HClO,2HClO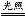 2HCl+O2↑,关系式为2Cl2~O2,则20 mL Cl2充分光照后,量筒中剩余气体约10 mL,故B正确;氯气与铜反应生成棕黄色的烟,加水溶液呈蓝色,故C错误;湿润的有色布条能褪色,是由于发生Cl2+H2O
2HCl+O2↑,关系式为2Cl2~O2,则20 mL Cl2充分光照后,量筒中剩余气体约10 mL,故B正确;氯气与铜反应生成棕黄色的烟,加水溶液呈蓝色,故C错误;湿润的有色布条能褪色,是由于发生Cl2+H2O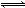 HCl+HClO,HClO具有漂白性,而干燥的氯气没有漂白性,故D错误。
HCl+HClO,HClO具有漂白性,而干燥的氯气没有漂白性,故D错误。
考点:氯气的生产原理和性质

练习册系列答案
相关题目