题目内容
下列A、B、C、D、E、F为几种常见仪器的部分结构(有的仪器只画出部分)
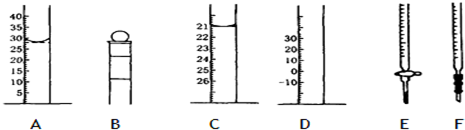
(1)A图中液面所示溶液的体积为 mL,C图中的液面与“0”刻度之间的体积差为 mL.
(2)仪器E的名称是 .
(3)Na2S2O3(硫代硫酸钠),俗称大苏打.把Na2S2O3?5H2O固体溶于水,得到无色溶液,该溶液显碱性,用离子反应方程式解释溶液显碱性的原因: .化工生产中常常依据反应2S2O32-+I2═S4O62-+2I-,用I2的标准溶液测定大苏打产品的纯度.步骤如下:
①称取5.5g Na2S2O3?5H2O产品,用仪器 (从上述A、B、C、D、E、F中选填)配制成100.00mL溶液.
②用仪器 (从上述A、B、C、D、E、F中选填)量取10.00mL溶液于锥形瓶中,以淀粉溶液为指示剂.
③用浓度为0.0500mol/L的I2标准溶液进行滴定,判断达到滴定终点的现象是 .
④重复滴定3次,数据记录于下表.计算所配制的Na2S2O3溶液的物质的量浓度为 (保留4位小数)mol/L,Na2S2O3?5H2O在产品中的质量百分数是 (保留1位小数).
⑤滴定时若用Na2S2O3溶液润洗锥形瓶,则测得大苏打产品的纯度 (填偏高、偏低、不变);若盛放I2标准液的滴定管下端有气泡,且在滴定过程中排出,则测得大苏打产品的纯度 .(填偏高、偏低、不变)

(1)A图中液面所示溶液的体积为
(2)仪器E的名称是
(3)Na2S2O3(硫代硫酸钠),俗称大苏打.把Na2S2O3?5H2O固体溶于水,得到无色溶液,该溶液显碱性,用离子反应方程式解释溶液显碱性的原因:
①称取5.5g Na2S2O3?5H2O产品,用仪器
②用仪器
③用浓度为0.0500mol/L的I2标准溶液进行滴定,判断达到滴定终点的现象是
| 编号 | 1 | 2 | 3 | 4 |
| Na2S2O3溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 20.01 | 20.02 |
⑤滴定时若用Na2S2O3溶液润洗锥形瓶,则测得大苏打产品的纯度
考点:中和滴定,探究物质的组成或测量物质的含量
专题:实验题
分析:(1)A为量筒,根据量筒的构造及液面的凹液面物质读出溶液体积;C为滴定管,0刻度在上方,图示液面位于21.00mL处;
(2)根据仪器B的构造写出其名称;
(3)S2O32?离子在溶液中水解导致溶液显示碱性;
①配制判断浓度的溶液需要使用容量瓶,B为容量瓶;
②Na2S2O3溶液显示碱性,需要使用碱式滴定管盛放;
③根据反应结束前溶液为无色、滴定结束时溶液显示蓝色判断滴定终点;
④先根据滴定消耗的标准液的体积计算出平均体积,然后根据反应2S2O32-+I2═S4O62-+2I-计算出10mL待测液中Na2S2O3溶液的物质的量及浓度;根据计算出的待测液的浓度计算出硫代硫酸钠晶体的质量,再计算出Na2S2O3?5H2O在产品中的质量百分数;
⑤锥形瓶不能润洗,若用Na2S2O3溶液润洗锥形瓶,会导致测定的待测液浓度偏高,测定结果偏高;
滴定时滴定管需要赶气泡,若盛放I2标准液的滴定管下端有气泡,导致消耗的标准液体积偏大,计算出的待测液浓度偏高.
(2)根据仪器B的构造写出其名称;
(3)S2O32?离子在溶液中水解导致溶液显示碱性;
①配制判断浓度的溶液需要使用容量瓶,B为容量瓶;
②Na2S2O3溶液显示碱性,需要使用碱式滴定管盛放;
③根据反应结束前溶液为无色、滴定结束时溶液显示蓝色判断滴定终点;
④先根据滴定消耗的标准液的体积计算出平均体积,然后根据反应2S2O32-+I2═S4O62-+2I-计算出10mL待测液中Na2S2O3溶液的物质的量及浓度;根据计算出的待测液的浓度计算出硫代硫酸钠晶体的质量,再计算出Na2S2O3?5H2O在产品中的质量百分数;
⑤锥形瓶不能润洗,若用Na2S2O3溶液润洗锥形瓶,会导致测定的待测液浓度偏高,测定结果偏高;
滴定时滴定管需要赶气泡,若盛放I2标准液的滴定管下端有气泡,导致消耗的标准液体积偏大,计算出的待测液浓度偏高.
解答:
解:(1)A为量筒,图中液面所示溶液的体积为28.0mL;C为滴定管,图中的液面读数为21.00mL,来与“0”刻度之间的体积差为21.00mL,
故答案为:28.0;21.00;
(2)仪器B下面带有玻璃旋塞,所以仪器B为酸式滴定管,
故答案为:酸式滴定管;
(3)S2O32?离子水解:S2O32?+5H2O?HS2O3?+0H?,导致溶液显示碱性,
故答案为:S2O32?+5H2O?HS2O3?+0H?;
①配制一定物质的量浓度的溶液,需要使用容量瓶进行配制,B为容量瓶,
故答案为:B;
②Na2S2O3溶液显示碱性,需要使用碱式滴定管量取,E为酸式滴定管、F为碱式滴定管,所以应该使用F量取,
故答案为:F;
③用浓度为0.0500mol/L的I2标准溶液进行滴定,滴定结束前碘单质没有剩余,溶液为无色,滴定结束时碘单质过量,溶液变成蓝色,则滴定终点的现象为:锥形瓶中的溶液由无色溶液变成蓝色,且半分钟不褪色,
故答案为:锥形瓶中的溶液由无色溶液变成蓝色,且半分钟不褪色;
④滴定过程中消耗I2标准溶液的平均体积为:
mL=20.00mL,10mL待测液消耗的碘单质的物质的量为:n(I2)=0.0500mol/L×0.02L=0.001mol,根据反应2S2O32-+I2═S4O62-+2I-可知,10mL待测液中含有的硫代硫酸钠的物质的量为:n(S2O32-)=2n(I2)=0.002mol,待测液的浓度为:c=
=0.2mol/L;
5.5g Na2S2O3?5H2O产品配制的100mL溶液中含有硫代硫酸钠的物质的量为:0.2mol/L×0.1L=0.02mol,含有 Na2S2O3?5H2O的质量为:248g/moL×0.02mol=4.96g,Na2S2O3?5H2O在产品中的质量百分数为:
×100%≈90.2%,
故答案为:0.2;90.2%;
⑤滴定时若用Na2S2O3溶液润洗锥形瓶,滴定时消耗的标准液体积偏大,测定的待测液浓度偏高,计算出的硫代硫酸钠晶体的质量偏大,则测得大苏打产品的纯度偏高;
若盛放I2标准液的滴定管下端有气泡,且在滴定过程中排出,测定的待测液浓度偏高,计算出的硫代硫酸钠晶体的物质的量偏大,则测得大苏打产品的纯度偏高,
故答案为:偏高;偏高.
故答案为:28.0;21.00;
(2)仪器B下面带有玻璃旋塞,所以仪器B为酸式滴定管,
故答案为:酸式滴定管;
(3)S2O32?离子水解:S2O32?+5H2O?HS2O3?+0H?,导致溶液显示碱性,
故答案为:S2O32?+5H2O?HS2O3?+0H?;
①配制一定物质的量浓度的溶液,需要使用容量瓶进行配制,B为容量瓶,
故答案为:B;
②Na2S2O3溶液显示碱性,需要使用碱式滴定管量取,E为酸式滴定管、F为碱式滴定管,所以应该使用F量取,
故答案为:F;
③用浓度为0.0500mol/L的I2标准溶液进行滴定,滴定结束前碘单质没有剩余,溶液为无色,滴定结束时碘单质过量,溶液变成蓝色,则滴定终点的现象为:锥形瓶中的溶液由无色溶液变成蓝色,且半分钟不褪色,
故答案为:锥形瓶中的溶液由无色溶液变成蓝色,且半分钟不褪色;
④滴定过程中消耗I2标准溶液的平均体积为:
| 19.99+19.98+20.01+20.02 |
| 4 |
| 0.002mol |
| 0.101L |
5.5g Na2S2O3?5H2O产品配制的100mL溶液中含有硫代硫酸钠的物质的量为:0.2mol/L×0.1L=0.02mol,含有 Na2S2O3?5H2O的质量为:248g/moL×0.02mol=4.96g,Na2S2O3?5H2O在产品中的质量百分数为:
| 4.96g |
| 5.5g |
故答案为:0.2;90.2%;
⑤滴定时若用Na2S2O3溶液润洗锥形瓶,滴定时消耗的标准液体积偏大,测定的待测液浓度偏高,计算出的硫代硫酸钠晶体的质量偏大,则测得大苏打产品的纯度偏高;
若盛放I2标准液的滴定管下端有气泡,且在滴定过程中排出,测定的待测液浓度偏高,计算出的硫代硫酸钠晶体的物质的量偏大,则测得大苏打产品的纯度偏高,
故答案为:偏高;偏高.
点评:本题考查了中和滴定操作方法及计算、计量仪器的构造及使用方法,题目难度中等,试题涉及的题量较大,注意掌握中和滴定操作方法,能够根据指示剂特点及反应原理正确判断滴定终点.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
下列各有机物中,属于烃的是( )
| A、氯丁烷 |
| B、苯 |
| C、硝基苯 |
| D、乙醇(CH3CH2OH) |
据报道,月球的土壤中吸附着数百万吨的32He,在地球上,氦元素主要以
He的形式存在.下列说法正确的是( )
4 2 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列对于NaHSO4的分类中不正确的是( )
| A、NaHSO4是盐 |
| B、NaHSO4是酸式盐 |
| C、NaHSO4是钠盐 |
| D、NaHSO4是酸 |
下列原子中,与氧元素原子化学性质相似的是( )
A、 氖 |
B、 碳 |
C、 镁 |
D、 硫 |
 常温下,用0.1000mol?L-1 NaOH溶液滴定20.00mL 0.1000mol?L-1 HClO溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用0.1000mol?L-1 NaOH溶液滴定20.00mL 0.1000mol?L-1 HClO溶液所得滴定曲线如图.下列说法正确的是( )| A、点①所示溶液中:c(ClO-)+c(OH-)=c(HClO)+c(H+) |
| B、点②所示溶液中:c(Na+)=c(HClO)+c(ClO-) |
| C、点③所示溶液中:c(Na+)>c(OH-)>c(ClO-)>c(H+) |
| D、滴定过程中可能出现:c(HClO)>c(ClO-)>c(H+)>c(Na+)>c(OH-) |
