题目内容
在标况下,2.24L NOx气体的质量为3g则x值为( )
| A、1 | B、2 | C、3 | D、4 |
考点:物质的量的相关计算
专题:推断题
分析:结合n=
、M=
及相对分子质量计算解答.
| V |
| Vm |
| m |
| n |
解答:
解:在标况下,2.24L NOx气体的质量为3g,则n(NOx)=
=0.1mol,
M(NOx)=
30g/mol,
其相对分子质量为30,则14+16x=30,解得x=1,
故选A.
| 2.24L |
| 22.4L/mol |
M(NOx)=
| 3g |
| 0.1mol |
其相对分子质量为30,则14+16x=30,解得x=1,
故选A.
点评:本题考查物质的量的计算,为高频考点,把握质量、物质的量、体积的关系为解答的关键,侧重基础知识的考查,题目难度不大.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
下列化学反应中,属于氧化还原的化合反应是( )
| A、Na2CO3+CaCl2═CaCO3↓+2NaCl | ||||
| B、Fe+CuSO4═Cu+FeSO4 | ||||
C、2NaHCO3
| ||||
| D、Na2O2+SO2═Na2SO4 |
与图中相对应的叙述是( )
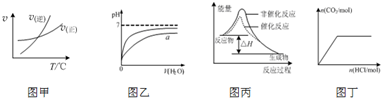

| A、由图甲表示的反应速率随温度变化的关系可知该反应的△H>0 |
| B、图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸 |
| C、图丙表示该反应为放热反应,且催化剂能改变反应的焓变 |
| D、图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系 |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )
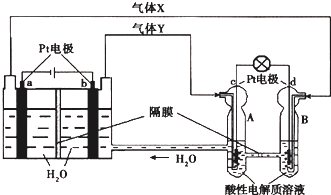

| A、当有0.1mol电子转移时,a极产生0.56L O2(标准状况下) |
| B、为了增加导电性可以将左边容器中的水改为食盐水 |
| C、c极上进行还原反应,B中的H+可以通过隔膜进入A |
| D、d极上发生的电极反应是:O2+4H++4e-═2H2O |
下列说法不正确的是( )
| A、离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | ||
| B、人造纤维可利用竹子、棉花、麻类的纤维材料制成,而合成纤维是利用自然界的非纤维材料(如石油、煤)通过化学合成方法得到 | ||
| C、有机玻璃是以有机物A(甲基丙烯酸甲酯)为单体,通过加聚反应得到,合成A的一种途经是: CH3C≡CH+CO+CH3OH
 ,其过程符合绿色化学的原则 ,其过程符合绿色化学的原则 | ||
| D、温室效应导致海水的酸度增加,珊瑚、贝壳类等生物的生存将会受到威胁 |
下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是( )
| A、a原子的最外层电子数比b原子的最外层电子数少 |
| B、把a、b两块金属片浸入稀硫酸中,用导线相连组成原电池时,电流由 a到b |
| C、1mol a从酸中置换H+生成的H2比1mol b从酸中置换H+生成的H2多 |
| D、常温时,a能从水中置换出氢,而b不能 |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B、28g乙烯所含共用电子对数目为4NA |
| C、1mol甲基的电子数目为7NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
下列有关晶体的说法中一定正确的是( )
①依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体;
②由原子直接构成的晶体就是原子晶体;
③分子晶体的堆积均采取分子密堆积;
④NaF、MgF2、SiF4三种晶体的熔点依次升高;
⑤金属键只存在于金属晶体中;
⑥离子键只存在于离子晶体中;
⑦H2O的性质非常稳定,原因在于分子之间存在氢键;
⑧SO2和SiO2晶体在熔化时破坏的作用力相同.
①依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体;
②由原子直接构成的晶体就是原子晶体;
③分子晶体的堆积均采取分子密堆积;
④NaF、MgF2、SiF4三种晶体的熔点依次升高;
⑤金属键只存在于金属晶体中;
⑥离子键只存在于离子晶体中;
⑦H2O的性质非常稳定,原因在于分子之间存在氢键;
⑧SO2和SiO2晶体在熔化时破坏的作用力相同.
| A、①⑤⑥⑦ | B、只有⑥ |
| C、②③⑤⑥ | D、①②⑤⑧ |
等物质的量的下列各有机物完全燃烧,生成CO2和H2O,耗氧量最多的是( )
| A、CH4O |
| B、C2H4O2 |
| C、C6H6 |
| D、C4H10 |