题目内容
下列与含氯化合物有关的说法正确的是( )
| A、随着化合价的升高,氯的含氧酸酸性和氧化性均逐渐增强 |
| B、向漂白粉中加入浓盐酸能产生黄绿色气体 |
| C、熔融氯化铝不导电,氯化铝溶液能导电,所以氯化铝是离子化合物 |
| D、检验Cl2中是否混有HCl,可以用湿润的淀粉-KI试纸 |
考点:氯、溴、碘及其化合物的综合应用
专题:元素及其化合物
分析:A、随着化合价的升高,氯的含氧酸酸性增强,氧化性逐渐减弱;
B、次氯酸钙和浓盐酸反应发生归中反应生成氯气;
C、氯化铝是共价化合物;
D、氯气与KI反应生成碘,而HCl不能与KI反应,则不能检验杂质.
B、次氯酸钙和浓盐酸反应发生归中反应生成氯气;
C、氯化铝是共价化合物;
D、氯气与KI反应生成碘,而HCl不能与KI反应,则不能检验杂质.
解答:
解:A、随着化合价的升高,氯的含氧酸酸性增强,氧化性逐渐减弱,故A错误;
B、次氯酸钙和浓盐酸反应发生氧化还原的归中反应,次氯酸根离子和氯离子在酸溶液中反应生成氯气,故B正确;
C、氯化铝是共价化合物,熔融氯化铝不导电,氯化铝溶液能导电,氯化铝是水分子作用下电离出离子,故C错误;
D、氯气与KI反应生成碘,而HCl不能与KI反应,则不能检验杂质,故D错误;
故选B.
B、次氯酸钙和浓盐酸反应发生氧化还原的归中反应,次氯酸根离子和氯离子在酸溶液中反应生成氯气,故B正确;
C、氯化铝是共价化合物,熔融氯化铝不导电,氯化铝溶液能导电,氯化铝是水分子作用下电离出离子,故C错误;
D、氯气与KI反应生成碘,而HCl不能与KI反应,则不能检验杂质,故D错误;
故选B.
点评:本题考查了物质性质和反应过程分析应用,注意氧化还原反应的理解,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
用10ml 0.1mol/L的AgNO3溶液恰好与相同体积的NaCl、MgCl2和AlCl3三种溶液完全反应,则这三种盐酸盐溶液的物质的量浓度之比是( )
| A、3:2:2 |
| B、6:3:2 |
| C、1:3:3 |
| D、3:1:1 |
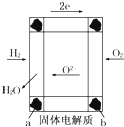 据报道,科学家已经研制出固体氧化物燃料电池,该电池以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,其工作原理如图所示(多孔电极a、b均不参加电极反应).下列说法正确的是( )
据报道,科学家已经研制出固体氧化物燃料电池,该电池以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,其工作原理如图所示(多孔电极a、b均不参加电极反应).下列说法正确的是( )| A、有H2O放出的a极为电池的正极 |
| B、b极对应的电极反应式为:O2+4e-+2H2O-→4OH- |
| C、正极对应的电极反应式为:O2+4H++4e--→2H2O |
| D、该电池的总反应式为:2H2+O2═2H2O |
ClO2是一种广谱消毒剂,根据世界环保联盟的要求ClO2将取代Cl2成为生产自来水的消毒剂(Cl2能和水中溶解的某些有机物发生取代和加成反应,生成致癌物质).工业上常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得ClO2,以上反应中NaClO3和Na2SO3的物质的量比为 ( )
| A、1:1 | B、2:1 |
| C、1:2 | D、2:3 |
已知CO和C的燃烧热分别是110.5kJ?mol-1、393.5kJ?mol-1.则 3.6g碳在6.4g氧气中燃烧至反应物耗尽时比3.6g碳在氧气中完全燃烧时少放出的热量是( )
| A、47.8kJ |
| B、22.1 kJ |
| C、56.2kJ |
| D、18.5kJ |
小明因体内缺乏维生素A患了夜盲症,同学们纷纷地给他补充维生素A的食谱.下列食品对补充维生素A没有明显作用的是( )
| A、鱼肝油 | B、蛋黄 |
| C、绿叶蔬菜 | D、豆制品 |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、常温常压下,11.2L氧气含有的原子数目为NA |
| B、14gN2和N4组成的混合气体中含有的原子数为NA |
| C、0.1NA个二氧化碳分子所占体积约为2.24L |
| D、1mol/L CaCl2溶液中含有的氯离子数目为2NA |
下列物质的分类结果正确的是( )
| A、焦炉气-混合物 胆矾-纯净物 臭氧-单质 |
| B、纯碱-碱 硫化氢-酸 小苏打-酸式盐 |
| C、油脂-高分子化合物 纤维素-天然高分子化合物 有机玻璃-合成高分子化合物 |
| D、液氯-非电解质 硫酸钡-强电解质 醋酸-弱电解质 |
能源可分为一级能源和二级能源,自然界中以现成形式提供的能源称为一级能源,需依靠其他能源的能量间接制取的能源称为二级能源.氢气就是一种高效而没有污染的二级能源.据此判断,下列叙述正确的是( )
| A、天然气是二级能源 |
| B、石油是二级能源 |
| C、煤是一级能源 |
| D、焦炉煤气是一级能源 |