题目内容
(1)配制FeSO4溶液时,常加入少量Fe粉,目的是 ;常加入少量H2SO4,目的是 .
(2)PH=5的盐酸溶液,加水稀释1000倍,pH大约为 ;NaHCO3加热蒸干得到的固体物质是 .
(3)用离子方程式描述泡沫灭火器的工作原理 .
(2)PH=5的盐酸溶液,加水稀释1000倍,pH大约为
(3)用离子方程式描述泡沫灭火器的工作原理
考点:铁盐和亚铁盐的相互转变,pH的简单计算,盐类水解的应用
专题:元素及其化合物
分析:(1)亚铁离子不稳定易被氧化,铁可以和铁离子之间反应得到亚铁离子,铁离子在溶液中水解,使溶液显示酸性;
(2)酸碱无限稀释,pH值接近于7,碳酸氢钠受热易分解;
(3)铝离子和碳酸氢根离子双水解会得到沉淀和气体.
(2)酸碱无限稀释,pH值接近于7,碳酸氢钠受热易分解;
(3)铝离子和碳酸氢根离子双水解会得到沉淀和气体.
解答:
解:(1)配制FeSO4溶液时,亚铁离子不稳定易被氧化为铁离子,为了使氧化生成的Fe3+转化为Fe2+,防止Fe2+被氧化,可以加入金属铁,铁离子在溶液中水解,使溶液显示酸性,为了反应掉生成的Fe(OH)3,防止Fe2+水解,可以在硫酸亚铁溶液中加入硫酸,
故答案为:使氧化生成的Fe3+转化为Fe2+,防止Fe2+被氧化;反应掉生成的Fe(OH)3,防止Fe2+水解;
(2)PH=5的盐酸溶液,加水稀释1000倍,pH大约为7;碳酸氢钠受热易分解得到Na2CO3,NaHCO3加热蒸干得到的固体物质是碳酸钠,故答案为:Na2CO3;
(3)泡沫灭火器中的硫酸铝中的铝离子和碳酸氢钠中碳酸氢根离子会发生双水解反应得到大量的二氧化碳,用来灭火,即Al3+3HCO3-=Al(OH)3↓+CO2↑,故答案为:Al3+3HCO3-=Al(OH)3↓+CO2↑.
故答案为:使氧化生成的Fe3+转化为Fe2+,防止Fe2+被氧化;反应掉生成的Fe(OH)3,防止Fe2+水解;
(2)PH=5的盐酸溶液,加水稀释1000倍,pH大约为7;碳酸氢钠受热易分解得到Na2CO3,NaHCO3加热蒸干得到的固体物质是碳酸钠,故答案为:Na2CO3;
(3)泡沫灭火器中的硫酸铝中的铝离子和碳酸氢钠中碳酸氢根离子会发生双水解反应得到大量的二氧化碳,用来灭火,即Al3+3HCO3-=Al(OH)3↓+CO2↑,故答案为:Al3+3HCO3-=Al(OH)3↓+CO2↑.
点评:本题涉及物质的性质以及应用知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
用酒精灯加热下列溶液,蒸干后灼烧,所得固体与溶质成份相同的是( )
| A、FeCl3溶液 |
| B、NaHCO3溶液 |
| C、Na2SO3溶液 |
| D、CH3COONa溶液 |
下列各组离子不能在同一溶液中共存的是( )
| A、H+、Fe2+、Cl-、NO3- |
| B、Na+、NH4+、HCO3-、SO42- |
| C、NH4+、Ca2+、NO3-、Cl- |
| D、Na+、K+、SO42-、Cl- |
下列离子反应方程式正确的是( )
| A、碳酸氢钠溶液跟过量的饱和石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| B、向Ba(OH)2溶液中滴加NaHSO4溶液至溶液显中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- |
| D、澄清石灰水中通入少量CO2:Ca(OH)2+CO2═CaCO3↓+H2O |
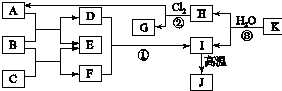 如图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源、燃料,J是一种耐高温材料且是两性氧化物,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出).
如图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源、燃料,J是一种耐高温材料且是两性氧化物,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出).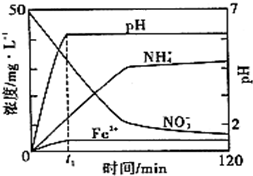 I.铁盐、亚铁盐是实验室常用的药品.
I.铁盐、亚铁盐是实验室常用的药品.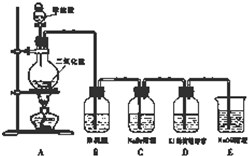 某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓)
某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓)